煤炭资源作为我国的主要天然能源,一直以来支撑着我国经济的发展。在煤炭开发与利用的过程中,伴生的煤矸石成为了我国排放量最大的工业副产物。我国煤矸石堆积存储量较多,自煤炭规模化开采以来煤矸石的累计排放量约50亿t,规模较大的煤矸石山1 900余座,占地面积约15 000 hm2,同时以每年1.5亿~2.0亿t的速度增加[1]。煤矸石中含有多种重金属元素、放射性元素等有害物质,在其露天堆放的过程中,经过风化、日晒、雨淋等作用,会发生一系列的生物、化学以及物理反应,使矸石中的有害物质被释放,这些污染物质的迁移会威胁到周围的地下水以及土壤环境 [2-3]。因此,目前相关研究极为重视煤矸石淋溶液对周边土壤、地下水等造成的影响,研究方法以动态淋溶或者静态浸泡为主,基于对溶出成分的分析评价作为标准,判断煤矸石淋滤过程中的环境效应[4-7]。
煤矸石成分复杂,含有多种重金属元素,由于重金属的毒性及其生物放大效应,过量重金属的存在干扰了地下水、土壤的有益利用[8-9]。目前,最适合的生物测定方法是利用发光菌来评估重金属毒性[10]。发光菌是一类在正常的生理条件下能够发射波长在450~490 nm的蓝绿色可见光的细菌,并且在一定的条件下发光强度恒定[11]。毒性物质会抑制发光菌的发光作用,因此研究中多利用发光菌来检测有毒物质。目前国内常用的发光菌包括明亮发光杆菌、费氏弧菌和青海弧菌。发光菌的生命周期短,对周围环境变化较为敏感[12],并且由于检测过程费时较少、灵敏度高、操作简便、结果准确等优点而受到重视,同时还有助于了解不同浓度梯度下的重金属毒性[13],因此在环境检测中的应用也越来越广泛,如工业废水与土壤中重金属污染的毒性检测以及农药残留毒性测试等[14-15]。
以贵州某酸性煤矸石堆为例,选用不同固液比及粒径为淋溶条件,通过对煤矸石的淋溶试验研究其![]() 以及重金属的淋溶规律,并利用明亮发光杆菌T3法对煤矸石的淋溶液进行生物毒性测试,进而分析煤矸石堆场对周围环境的影响。
以及重金属的淋溶规律,并利用明亮发光杆菌T3法对煤矸石的淋溶液进行生物毒性测试,进而分析煤矸石堆场对周围环境的影响。
试验所用的煤矸石样品采集于贵州某矿区的矸石堆场,采于较为分散的不同位置的采样点,采集后的煤矸石在实验室的阴凉通风处风干,得到混合粒径煤矸石样品。对混合粒径煤矸石进行筛分处理,得到小、中、大3种粒径的矸石样,其中小粒径<1 mm、中粒径1~10 mm、大粒径10~30 mm,煤矸石中主要的金属成分见表1。
表1 煤矸石中主要的金属成分
Table 1 Main metal ingredients in gangue
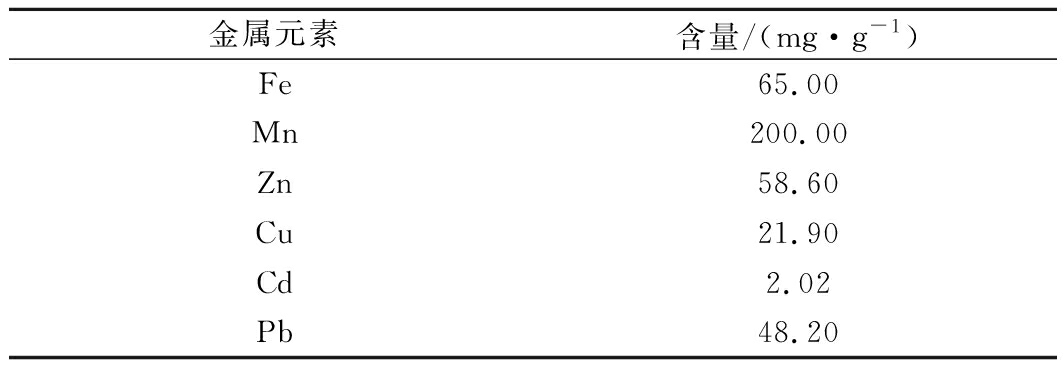
金属元素含量/(mg·g-1)Fe65.00Mn200.00Zn58.60Cu21.90Cd2.02Pb48.20
1)静态淋溶,称取10.0 g混合粒径的煤矸石置于100 mL烧杯中,分别向烧杯中注入20、40、80 mL去离子水,使浸泡实验的固液比分别为1∶2、1∶4、1∶8,振荡摇匀,浸泡0.5、1、2、4、8、12和24 h后,取上清液过0.45 μm滤膜后,进行各类指标测定。为探究不同粒径煤矸石静态淋溶特征,分别称取10.0 g小粒径、中粒径和大粒径的煤矸石置于100 mL烧杯中,注入20 mL去离子水,振荡摇匀,浸泡0.5、1、2、4、8、12和24 h后,取上清液过0.45 μm滤膜后,进行各类指标测定。
2)动态淋溶,动态淋溶装置为PVC柱形管,管径5 mm,高10 mm。称取50 g不同粒径煤矸石样品置于PVC管中,并在底部和顶部分别铺设2 mm厚的石英砂(粒径为0.85~1.70 mm)。通过蠕动泵向装置中喷淋去离子水,蠕动泵的喷淋强度设为0.36 mL/min。以装置出水时开始计时,连续喷淋24 h。在3、6、12、18、24 h时分别取样,进行各类指标测定。
利用明亮发光杆菌T3法,将上述动态淋溶试验中,淋溶3 h后的淋溶液及稀释100倍的淋溶液进行明亮发光菌急性毒性测试,该法以水样的相对发光度来表示水样的毒性水平,急性毒性的分级标准见表2[16]。使用菌种为明亮发光杆菌T3小种(Photobacterium phoshoreum T3 spp.)冻干粉,水质急性毒性水平选用相当的参比物氯化汞来表征。试验所用仪器:Glomax Multi型微孔板型多功能检测仪、BL22-500A超声波清洗机、96孔细胞培养板。
表 2 发光细菌法测定水质毒性的分级标准
Table 2 Standard for classification of water toxicity by luminescent bacteria method

等级相对发光强度/%毒性等级Ⅰ>70低毒Ⅱ50~70中毒Ⅲ30~50重毒Ⅳ0~30高毒Ⅴ0剧毒
1.3.1 明亮发光杆菌的复苏
将明亮发光杆菌T3冻干粉按照国标[17]进行复苏。取出含有0.2 g发光细菌冻干粉安瓿瓶和氯化钠溶液,放入置有冰块的小号(1.0~1.5 L)保温瓶,用l mL注射器吸取l mL冷的氯化钠 (10-2 g/mL) 注入已开口的冻干粉西林瓶,充分混匀。2 min后,细菌复苏并发光(可在暗室内检验,肉眼应见微光),备用。取复苏后的发光菌液0.1 mL,用2.5%氯化钠溶液稀释到10 mL,使用微孔多功能检测仪测定初始发光强度。
1.3.2 分析方法
将每个样品设置3个平行。同时设置96孔板第1行为阴性质控,第2行为阳性质控。各孔中加入样品液180 μL和菌液20 μL,总体积为200 μL。放入仪器进行测试,以此为样品初始发光强度记做S0;记录阴性质控(3% NaCl)初始发光强度为C0;阳性质控(0.1 mg/L氯化汞)当做样品处理。
设置15 min的反应时间,然后使用微孔板型多功能检测仪测定受试样品中发光菌的发光强度,记录t时刻,阴性质控初始发光强度为Ct;样品初始发光强度记做St;相对发光度记作T;阳性质控当做样品处理,初始发光强度记作Pt。根据测定结果计算相对发光度(%),并算出平均值。
T=St/Ct×100%
(1)
2.1.1 煤矸石固液比对重金属释放的影响
将混合粒径的煤矸石分别以1∶2、1∶4、1∶8的固液比进行静态淋溶试验,固液比对pH以及硫酸根、各金属含量的影响如图1和图2所示。不同固液比下,浸出液的pH随时间增加均表现出显著的下降趋势,浸泡时间分别为1 h和8 h时,降低最为明显。固液比为1∶8时的pH明显大于1∶2和1∶4时。pH值整体逐渐降低是由于氢离子对煤矸石矿相的侵蚀作用。Fe、Mn的浸出量最大且浸出规律较为相似,浸出量随时间的延长显著增加,且均在浸泡前期处于缓慢释放阶段,后期处于快速释放阶段,2者均属于较易释放元素。固液比为1∶2、1∶4、1∶8时,Fe、Mn的最大浸出率分别为0.23%、0.19%、0.07%和32.75%、28.55%、14.35%,可见固液比越大越利于重金属溶出。硫酸根的释放量在不同固液比下均存在显著差异,其含量表现为1∶2>1∶4>1∶8。
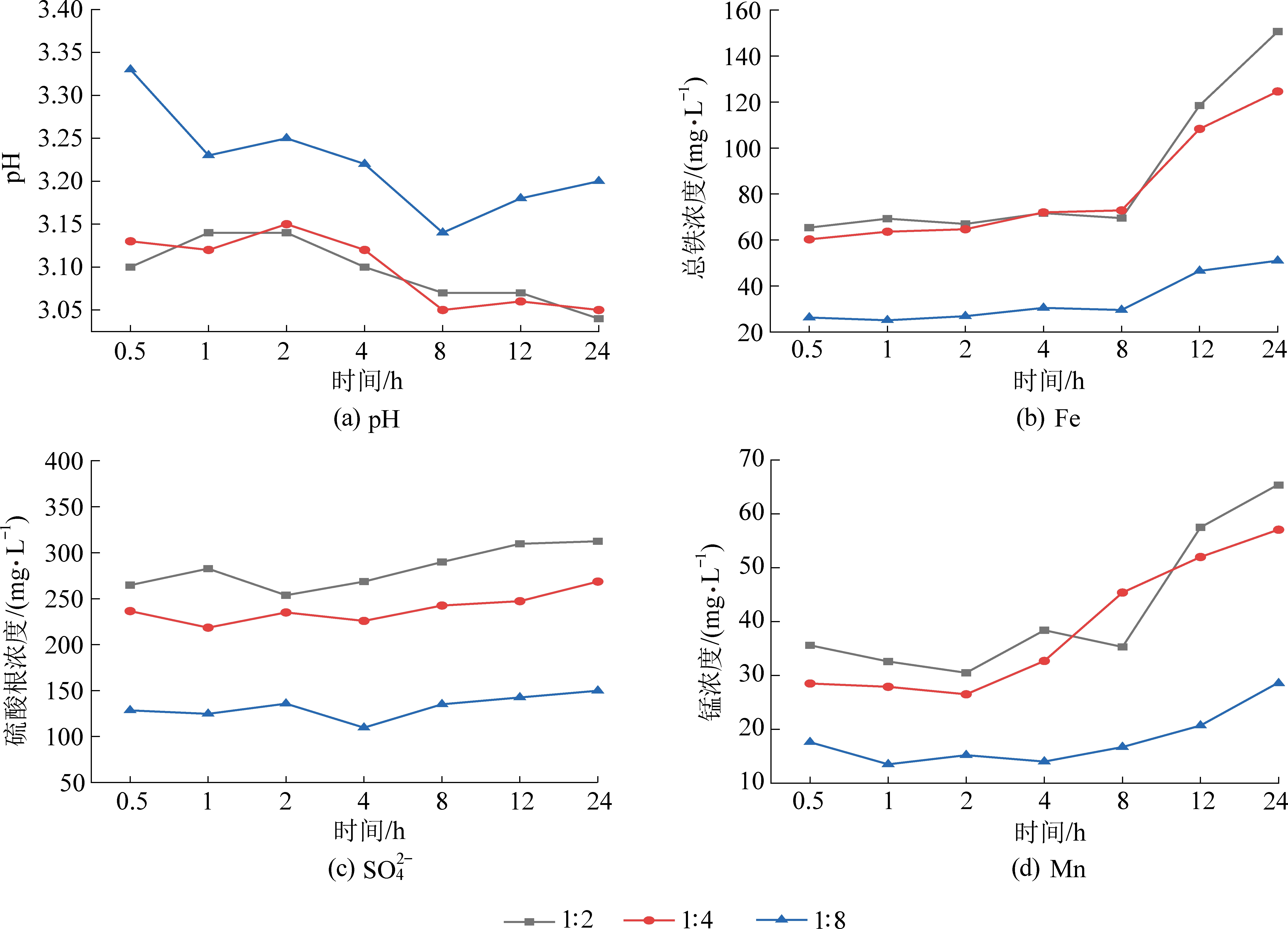
图1 不同固液比下煤矸石静态淋溶液pH值、Fe、Mn和![]() 浓度变化
浓度变化
Fig.1 Changes of pH values, Fe, Mn and ![]() contents in coal gangue static leaching solution with different solid-liquid ratios
contents in coal gangue static leaching solution with different solid-liquid ratios
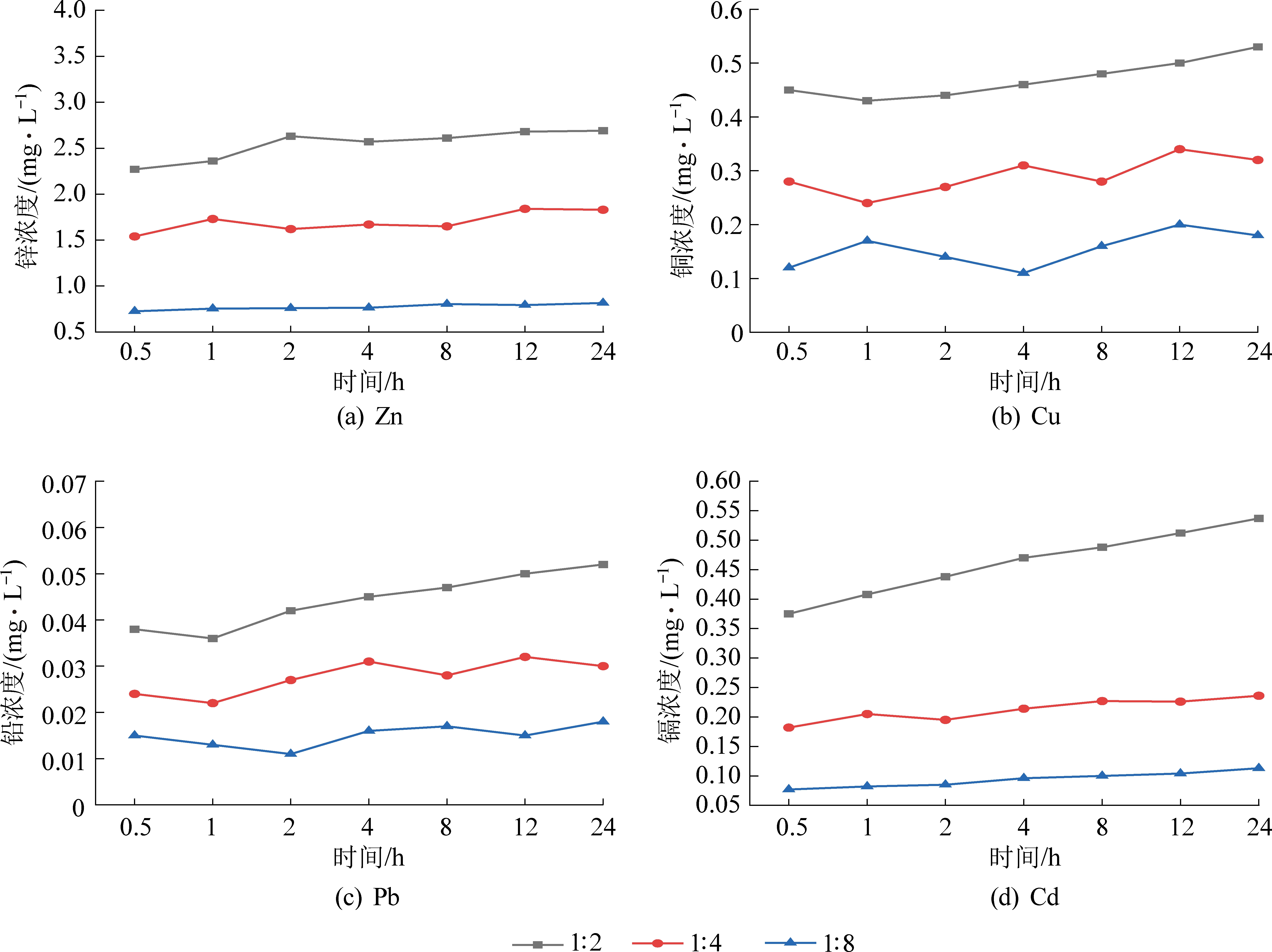
图2 不同固液比下煤矸石静态淋溶液重金属浓度变化
Fig.2 Changes of heavy metal content in coal gangue static leaching solution with different solid-liquid ratios
不同固液比条件下,Zn、Pb、Cu、Cd等4种重金属含量存在显著差异,均表现为1∶2>1∶4>1∶8。随着浸泡时间的增加,Zn、Cd含量变化略平缓,仅在极小范围内波动。Cu、Pb的释放较为复杂,属于间歇式释放,特别是在固液比为1∶4和1∶8时,浸出过程中Cu和Pb的释放量出现了2次峰值,第1次峰值的出现说明在浸泡前期,煤矸石中的易交换态的Cu、Pb被释放;第2次峰值的出现说明了煤矸石中Cu、Pb的存在形式除易交换态外还有氧化态和络合态。此结果与ZHANG等[18]所得结论相似。
2.1.2 煤矸石粒径对重金属释放的影响
分别对小粒径(<1 mm)、中粒径(1~10 mm)、大粒径(10~30 mm)3种煤矸石进行静态淋溶试验,结果如图3和图4所示,不同粒径煤矸石淋溶液的pH呈下降趋势,小粒径的pH值明显高于中粒径和大粒径,24 h内pH值的平均值依次为:中粒径(2.91 mm)<大粒径(2.96 mm)<小粒径(3.14 mm)。从稳定性角度分析可得,煤矸石的粒径越小,浸出液的稳定性越差,波动越明显。较不同固液比条件下浸出液的元素含量相比,煤矸石的粒径对元素释放的影响更大。Fe、Mn以及![]() 在不同粒径条件下的溶出浓度差异较大,这是由于煤矸石中的污染物释放的浓度梯度较高[19]。小、中、大3种粒径的淋出液中,Fe的最大溶出率分别为0.22%、0.25%、0.18%;Mn的最大溶出率分别为25.25%、33.57%、21.63%。不同粒径下Fe、Mn的静态溶出率表现为:中粒径>大粒径>小粒径;而对于
在不同粒径条件下的溶出浓度差异较大,这是由于煤矸石中的污染物释放的浓度梯度较高[19]。小、中、大3种粒径的淋出液中,Fe的最大溶出率分别为0.22%、0.25%、0.18%;Mn的最大溶出率分别为25.25%、33.57%、21.63%。不同粒径下Fe、Mn的静态溶出率表现为:中粒径>大粒径>小粒径;而对于![]() 可以明显观察到小粒径中溶出的
可以明显观察到小粒径中溶出的![]() 明显高于中粒径和大粒径。在24 h的淋溶过程中,Zn、Pb、Cu、Cd等4种金属的溶出量均呈现上升趋势,但不同粒径条件下各种金属含量的变化差异并不显著,小、中、大3种粒径的淋出液中,Zn和Pb均在中期达到最大溶出量,分别为3.11、3.27、3.01 mg/L和0.051、0.053、0.046 mg/L,相对应的溶出率为5.31%、5.58%、5.13%和0.10%、0.11%、0.095%;Cu和Cd均在淋溶后期达到最大溶出量,分别为0.52、0.56、0.48 mg/L和0.544、0.563、0.511 mg/L,相对应的溶出率为2.37%、2.56%、2.19%和26.93%、27.87%、25.29%。结果发现大粒径的煤矸石金属溶出率最低,中粒径略大于小粒径,所得结果异于ASHFAQ M、林海、何保等[20-22]得出的煤矸石粒度越小越利于重金属的溶出的结论,这可能是因为本次试验中的静态淋溶时间较短,重金属溶出的波动性较大,不能明确观察到金属溶出量和粒径之间的关系。
明显高于中粒径和大粒径。在24 h的淋溶过程中,Zn、Pb、Cu、Cd等4种金属的溶出量均呈现上升趋势,但不同粒径条件下各种金属含量的变化差异并不显著,小、中、大3种粒径的淋出液中,Zn和Pb均在中期达到最大溶出量,分别为3.11、3.27、3.01 mg/L和0.051、0.053、0.046 mg/L,相对应的溶出率为5.31%、5.58%、5.13%和0.10%、0.11%、0.095%;Cu和Cd均在淋溶后期达到最大溶出量,分别为0.52、0.56、0.48 mg/L和0.544、0.563、0.511 mg/L,相对应的溶出率为2.37%、2.56%、2.19%和26.93%、27.87%、25.29%。结果发现大粒径的煤矸石金属溶出率最低,中粒径略大于小粒径,所得结果异于ASHFAQ M、林海、何保等[20-22]得出的煤矸石粒度越小越利于重金属的溶出的结论,这可能是因为本次试验中的静态淋溶时间较短,重金属溶出的波动性较大,不能明确观察到金属溶出量和粒径之间的关系。
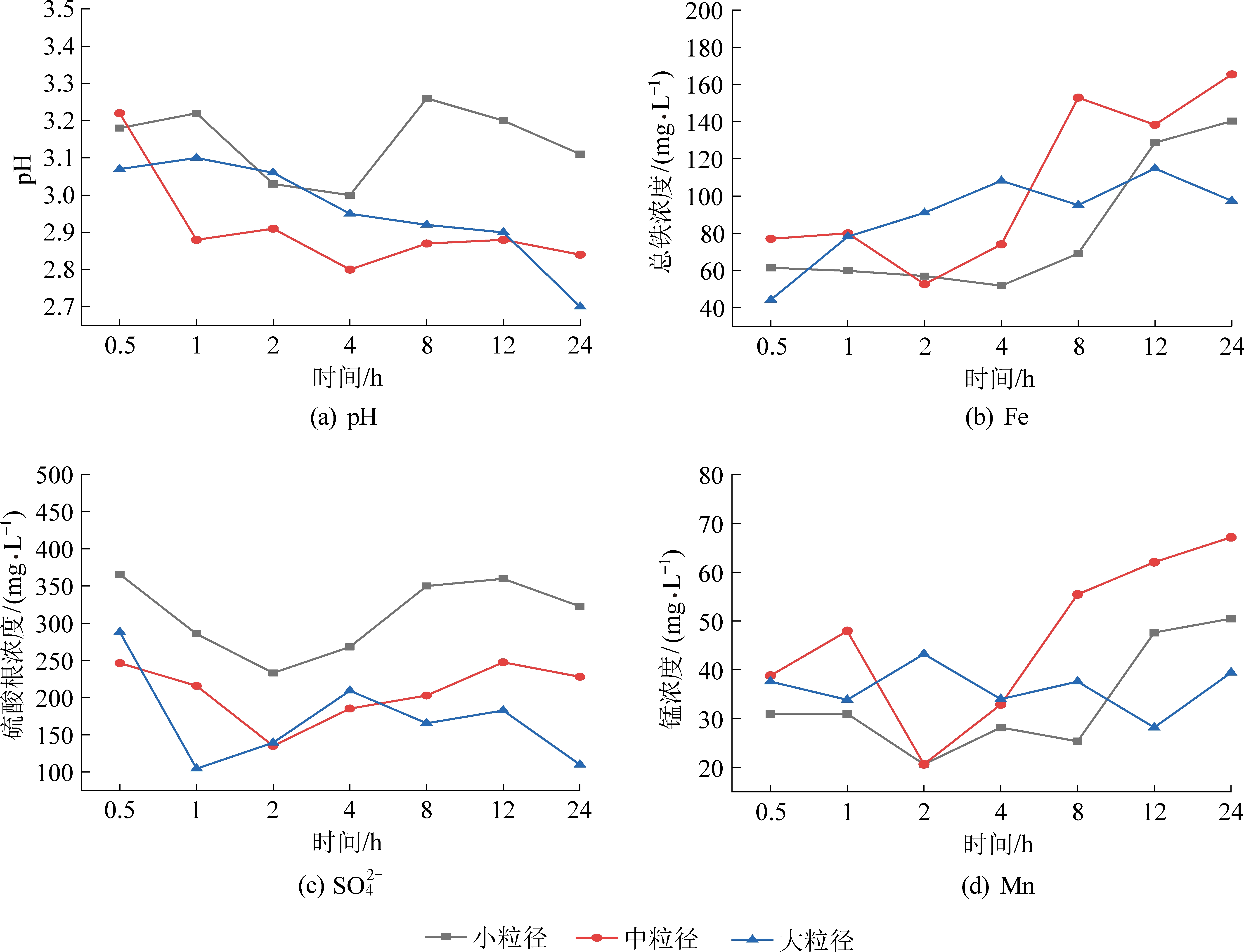
图3 不同粒径煤矸石静态淋溶液pH值、Fe、Mn和![]() 浓度变化
浓度变化
Fig.3 Changes of pH values, Fe, Mn and ![]() in static leaching solutions of gangue with different particle sizes
in static leaching solutions of gangue with different particle sizes
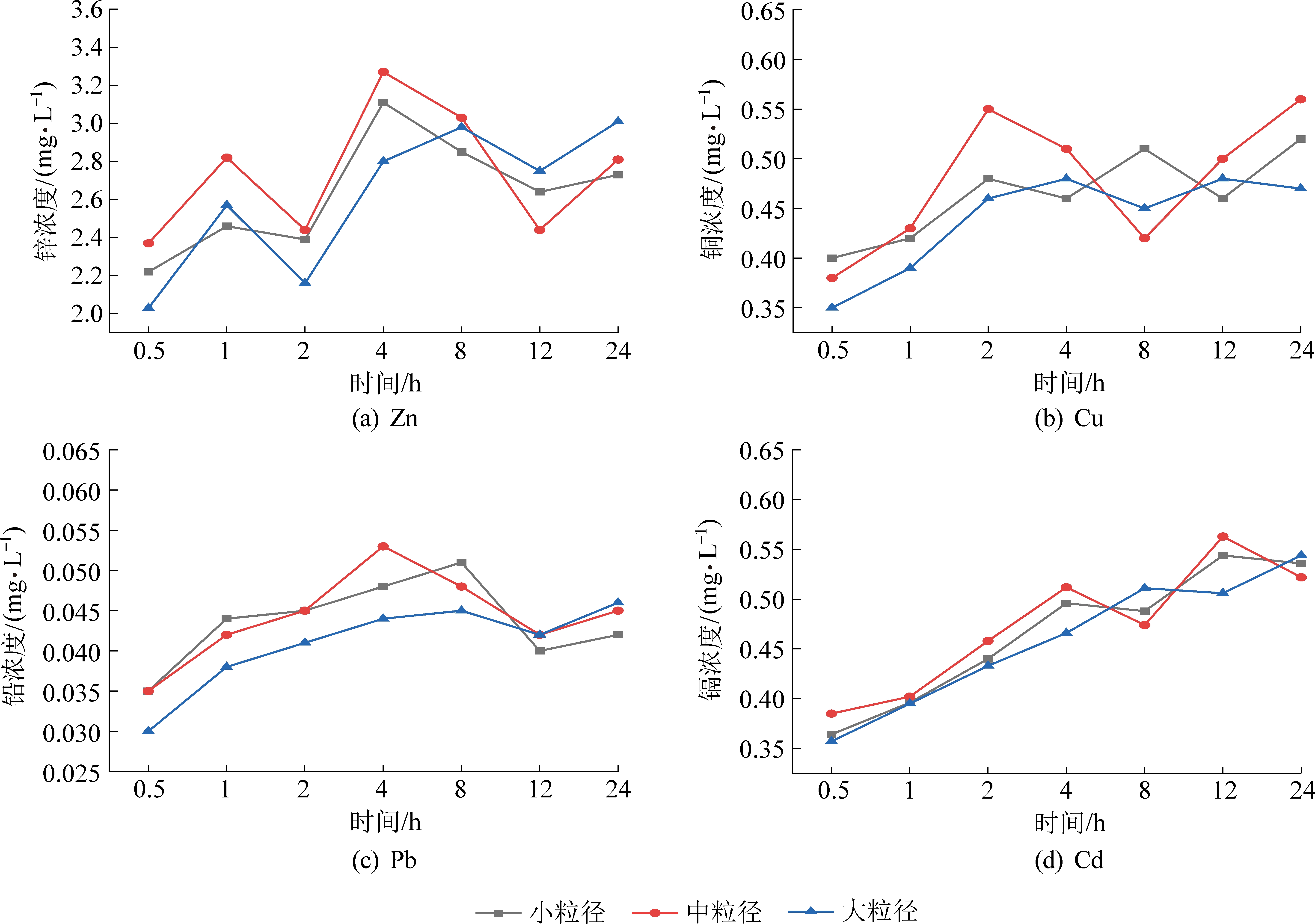
图4 不同粒径煤矸石静态淋溶液重金属浓度变化
Fig.4 Changes of heavy metal content in static leaching solution of gangue with different particle sizes
2.2.1 各重金属的淋溶规律
不同粒径煤矸石动态淋溶试验得到的淋溶液中各类指标变化趋势如图5、图6所示。随着淋溶时间的增加,不同粒径煤矸石动态淋溶液的pH不断增加,硫酸根和各重金属均在强酸环境下达到最大溶出量。![]() 变化趋势相似,淋溶过程中,不同粒径条件下的差异并不明显。相比之下Zn、Pb、Cu、Cd等4种金属在不同粒径条件下的变化表现出明显差异。淋溶初期淋出液酸性较强,强酸条件下可以观察到小粒径煤矸石中的Zn、Pb、Cu、Cd溶出量最大,随着淋出液pH的增加,4重金属元素的溶出量受粒径的影响逐渐减弱。整个淋溶过程中,Fe的溶出量最大,这是煤矸石中Fe的含量最大导致的;Mn的溶出率较大,最大高达71.1%,这可能是因为淋溶环境没有能够抑制Mn迁移的羟基氧化物和碳酸盐,从而导致其迁移能力较强,这与ASHFAQ M等[23]所得结果相似。Zn、Cu、Cd和Pb的溶出量较低,其中Pb的溶出量最低,煤矸石中Pb的含量相对于其他元素较高,但在酸性最强时的浸出率也仅有0.05%,这可能是由于Pb在煤矸石中的矿物形态使其在酸性环境下较稳定,不受水合氢离子的干扰[24]。
变化趋势相似,淋溶过程中,不同粒径条件下的差异并不明显。相比之下Zn、Pb、Cu、Cd等4种金属在不同粒径条件下的变化表现出明显差异。淋溶初期淋出液酸性较强,强酸条件下可以观察到小粒径煤矸石中的Zn、Pb、Cu、Cd溶出量最大,随着淋出液pH的增加,4重金属元素的溶出量受粒径的影响逐渐减弱。整个淋溶过程中,Fe的溶出量最大,这是煤矸石中Fe的含量最大导致的;Mn的溶出率较大,最大高达71.1%,这可能是因为淋溶环境没有能够抑制Mn迁移的羟基氧化物和碳酸盐,从而导致其迁移能力较强,这与ASHFAQ M等[23]所得结果相似。Zn、Cu、Cd和Pb的溶出量较低,其中Pb的溶出量最低,煤矸石中Pb的含量相对于其他元素较高,但在酸性最强时的浸出率也仅有0.05%,这可能是由于Pb在煤矸石中的矿物形态使其在酸性环境下较稳定,不受水合氢离子的干扰[24]。
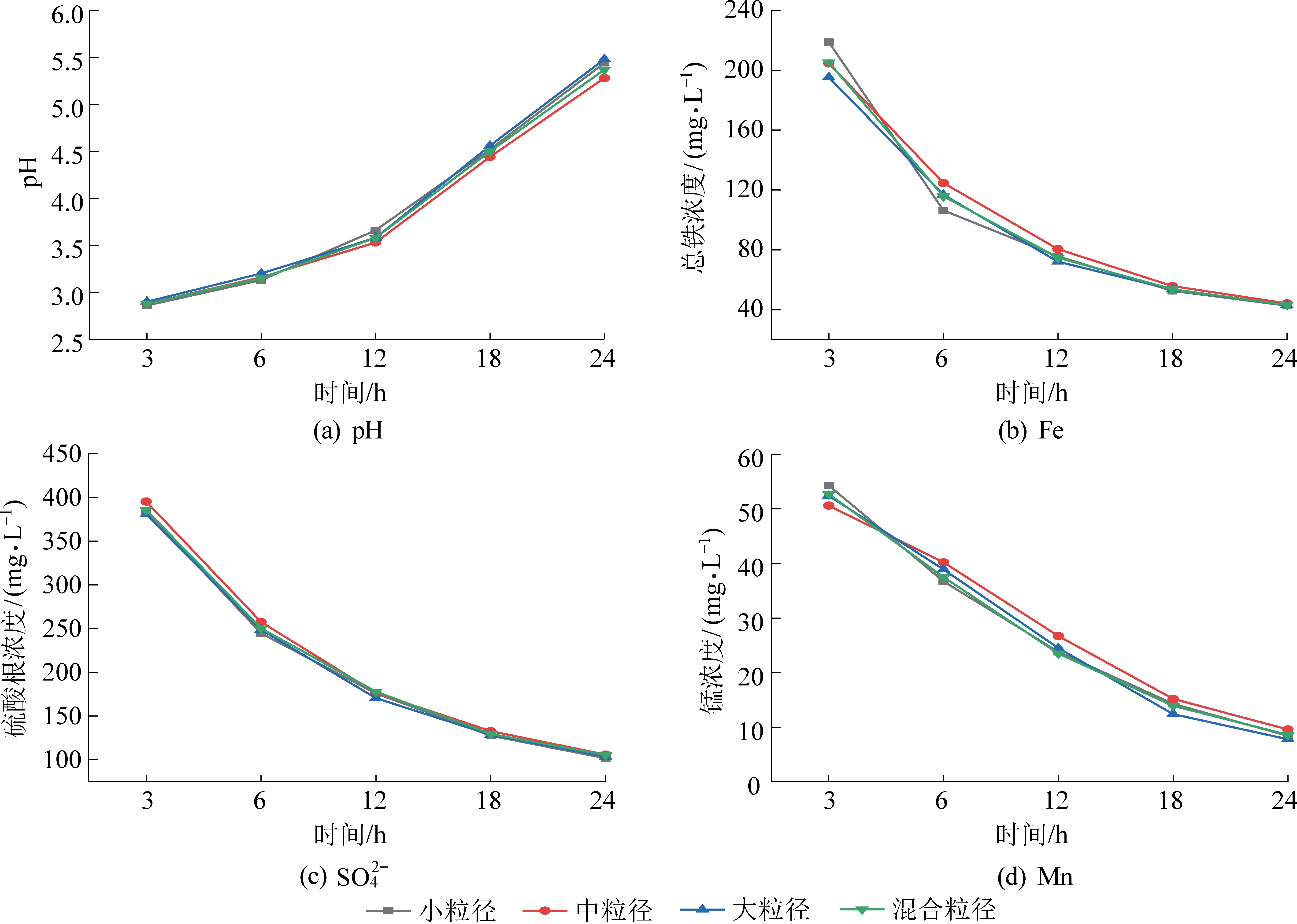
图5 不同粒径煤矸石动态淋溶液pH值、Fe、Mn和![]() 浓度变化
浓度变化
Fig.5 Changes of pH values, Fe, Mn and ![]() contents in dynamic leaching solutions of gangue with different particle sizes
contents in dynamic leaching solutions of gangue with different particle sizes
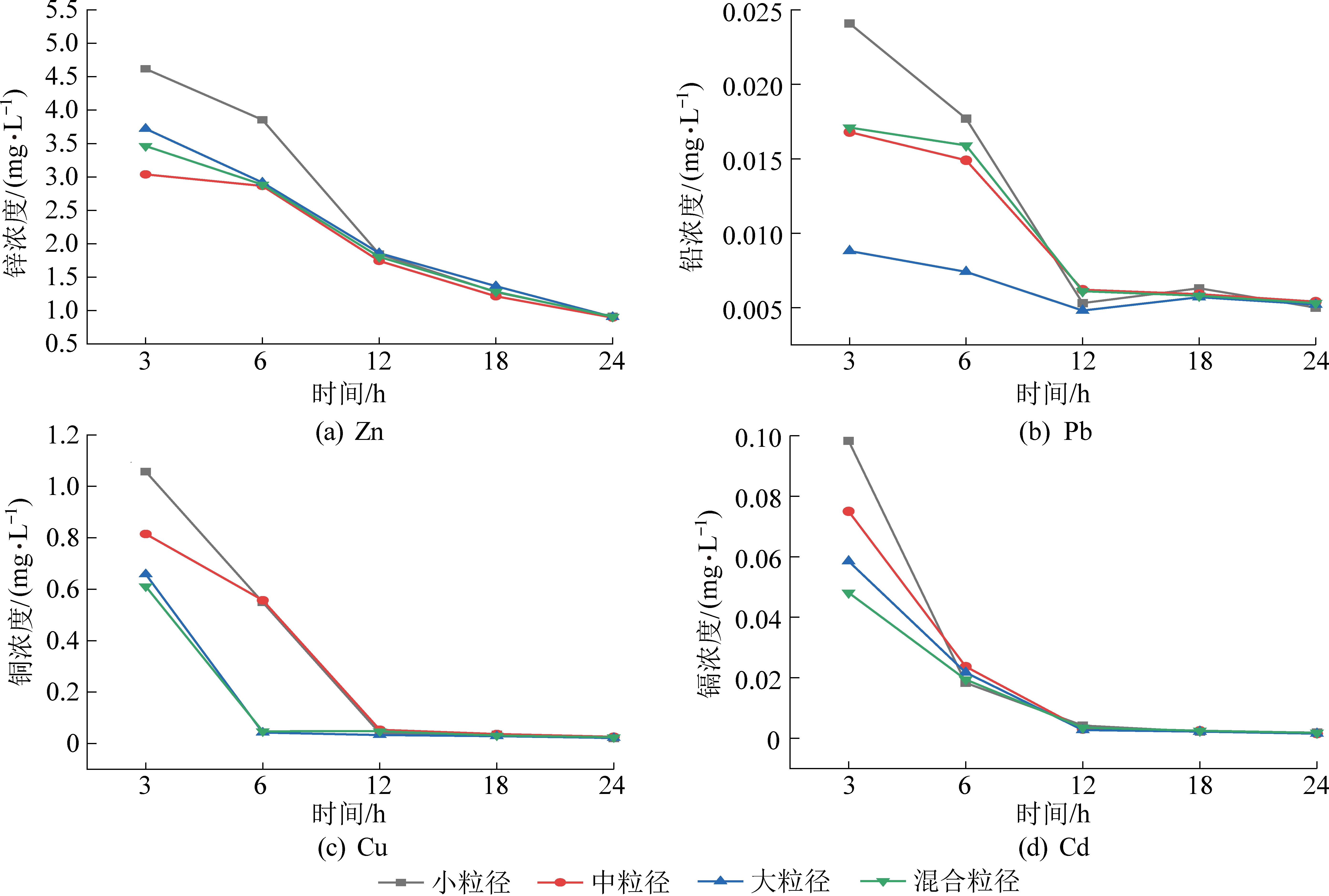
图6 不同粒径煤矸石动态淋溶液重金属浓度变化
Fig.6 Changes of heavy metal content in dynamic leaching solution of gangue with different particle sizes
2.2.2 煤矸石淋滤液中重金属的累计释放量
重金属的累计释放量是评价重金属危害的重要依据,表示在淋滤期间内的全部淋滤液中重金属的绝对质量。王心义等[25]在研究矸石堆放对土壤的重金属污染效应时,发现重金属的总量是一个必要的参数值,且其总量越高,对环境的危害就越大。煤矸石淋滤液中重金属的累计释放量计算公式:
(2)
式中:q为金属累计释放量;n为采样总次数;Ci为第i次采样淋出液中重金属的浓度;Vi为第i次淋出液的体积;m为柱内矸石质量。得到不同粒径淋溶液中重金属累计释放量见表3。
表3 煤矸石中重金属累计释放量
Table 3 Accumulated release of heavy metals in coal gangue
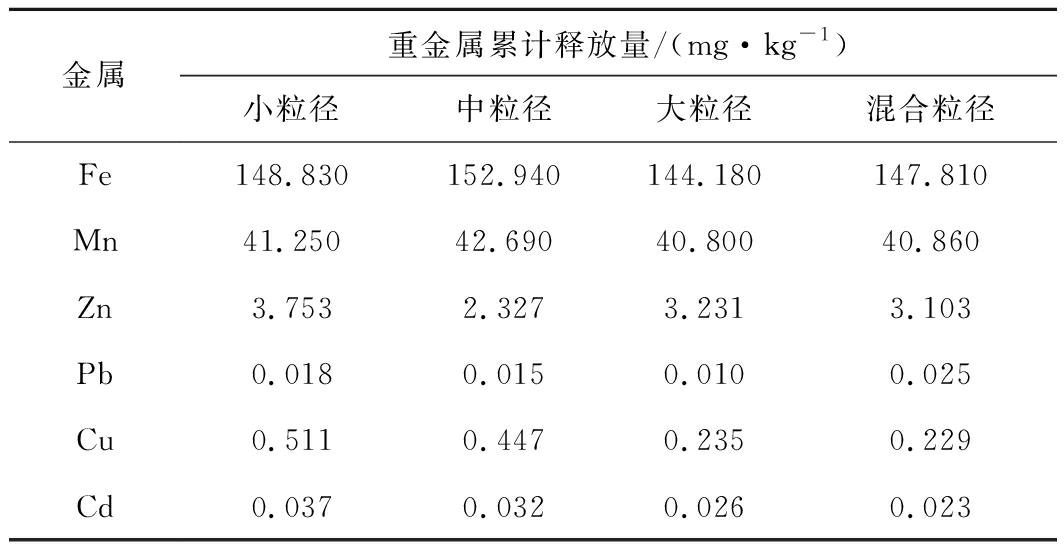
金属重金属累计释放量/(mg·kg-1)小粒径中粒径大粒径混合粒径Fe148.830152.940144.180147.810Mn41.25042.69040.80040.860Zn3.7532.3273.2313.103Pb0.0180.0150.0100.025Cu0.5110.4470.2350.229Cd0.0370.0320.0260.023
由表3可知,小、中、大3种粒径煤矸石的重金属累计释放量为Fe>Mn>Zn>Cu>Cd>Pb,而混合粒径煤矸石的重金属累计释放量为Fe>Mn>Zn>Cu>Pb>Cd 。对比各重金属在不同粒径条件下的累计释放量可发现,中粒径的Fe、Mn累计释放量最大,分别为152.940、42.690 mg/kg;小粒径的Zn、Cu、Cd累计释放量最大,分别为3.753、0.511、0.037 mg/kg。煤矸石的粒径对其中重金属的累计释放量存在影响。
2.2.3 煤矸石中各种金属的迁移方程
根据动态淋溶试验结果,利用2次回归方程对淋溶液中各重金属的释放量随时间的变化进行拟合。2次回归方程为:Y=A+B1x+B2x2。拟合结果见表4和表5。
表4 不同粒径煤矸石中各重金属释放量回归拟合
Table 4 Regression fitting for release of heavy metals in gangue with different particle sizes

重金属重金属释放量回归拟合小粒径煤矸石中粒径煤矸石FeY=327.42-131.8x+15.20x2R2=0.944 9Y=296.92-105.87x+11.15x2R2=0.993 8MnY=75.16-22.90x+1.91x2R2=0.999 8Y=66.36-15.67x+0.83x2 R2=0.986 0ZnY=6.61-1.95x+0.12x2R2=0.920 0Y=2.08-0.72x+0.021x2R2=0.899 4PbY=0.032-0.003x+7.9×10-5x2R2=0.938 1Y=0.023-0.001 8x+4.51×10-5x2R2=0.921 5CuY=1.86-0.89x+0.11x2R2=0.964 8Y=1.42-0.63x+0.070x2R2=0.897 8CdY=0.17-0.094x+0.012x2 R2=0.872 8Y=0.13-0.068x+0.008 6x2R2=0.950 5
表5 不同粒径煤矸石中各重金属释放量回归拟合
Table 5 Regression fitting for release of heavy metals in gangue with different particle sizes
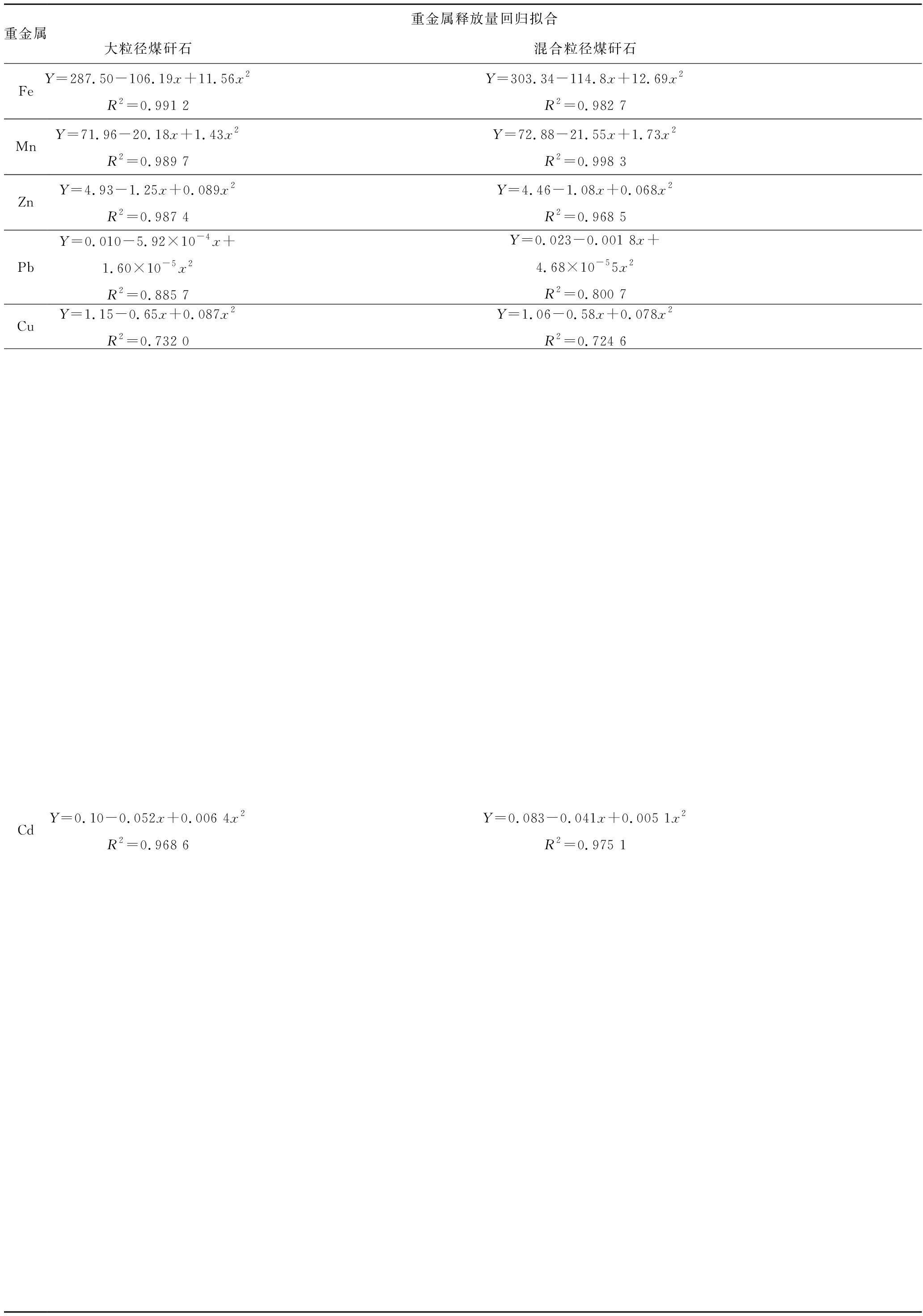
重金属重金属释放量回归拟合大粒径煤矸石混合粒径煤矸石FeY=287.50-106.19x+11.56x2R2=0.991 2Y=303.34-114.8x+12.69x2R2=0.982 7MnY=71.96-20.18x+1.43x2 R2=0.989 7Y=72.88-21.55x+1.73x2R2=0.998 3ZnY=4.93-1.25x+0.089x2R2=0.987 4Y=4.46-1.08x+0.068x2 R2=0.968 5PbY=0.010-5.92×10-4x+1.60×10-5x2R2=0.885 7Y=0.023-0.001 8x+4.68×10-55x2R2=0.800 7CuY=1.15-0.65x+0.087x2R2=0.732 0Y=1.06-0.58x+0.078x2R2=0.724 6CdY=0.10-0.052x+0.006 4x2 R2=0.968 6Y=0.083-0.041x+0.005 1x2R2=0.975 1
观察回归系数B1、B2,可以发现当淋溶小粒径煤矸石时,重金属的释放速率为Fe>Mn>Zn>Cu>Cd>Pb;淋溶中粒径煤矸石时,重金属释放速率为Fe>Mn>Cu>Zn>Cd>Pb;当淋溶大粒径煤矸石时,重金属释放速率为Fe>Mn>Cu>Zn>Cd>Pb;当淋溶混合粒径煤矸石时,重金属释放速率为Fe>Mn>Cu>Zn>Cd>Pb。煤矸石中的重金属释放速率并没有因其粒径的不同而呈现出较为明显的变化,这与李万鹏[26]所得结论相似。
根据拟合方程可知,重金属的溶出量随着淋溶时间的增长而增加,二者呈多项式关系[27]。淋溶初期重金属的释放速率较快,但随着淋溶时间的延长,重金属的溶出速率随之逐渐减缓,淋溶后期重金属以稳定释放的方式进行。因此,在煤矸石堆放的过程中,重金属的释放量会日渐达到平衡。
明亮发光菌急性毒性实验结果见表6,淋溶3 h后,淋溶液pH值较低、重金属含量较高。不同粒径煤矸石淋溶液的相对发光度均为0,属于剧毒溶液。稀释100倍后,各类污染物含量小于淋溶24 h后的淋溶液,然而其相对发光强度为60%左右,处于中毒水平。相对发光强度为中粒径<混合粒径<小粒径<大粒径,而相对发光强度越小,溶液所表现出的毒性越高,由此可知本次试验中,中粒径煤矸石淋溶液毒性最高。
表6 不同粒径煤矸石淋溶液急性毒性
Table 6 Acute toxicity of gangue leaching solutions with different particle sizes
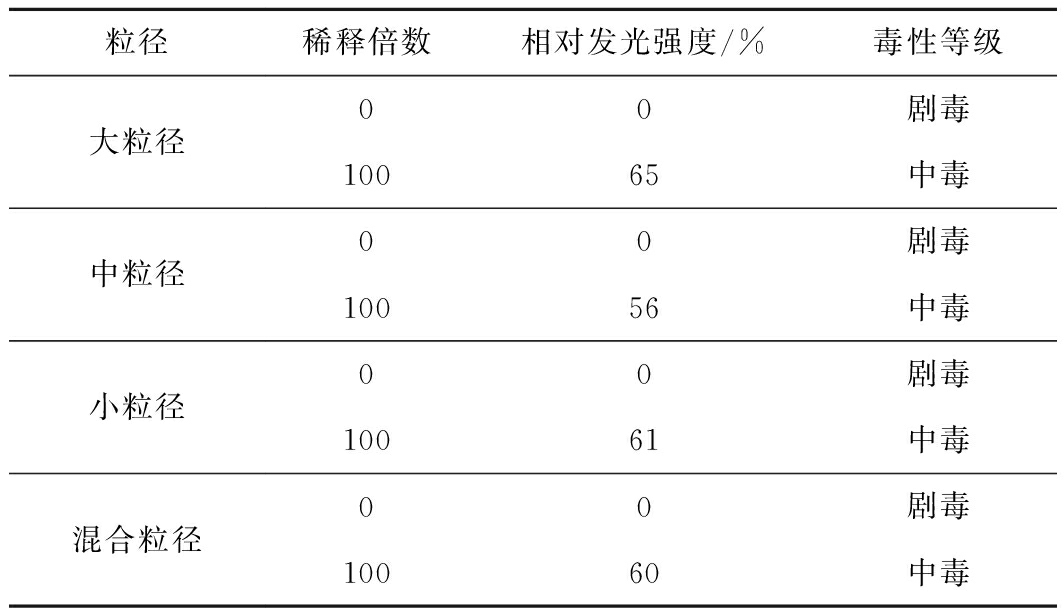
粒径稀释倍数相对发光强度/%毒性等级大粒径00剧毒10065中毒中粒径00剧毒10056中毒小粒径00剧毒10061中毒混合粒径00剧毒10060中毒
将煤矸石淋溶液重金属含量对明亮发光杆菌活性影响的相关性进行分析,结果见表7。可以看出6种重金属的含量均与菌活性为负相关,即均对其表现出抑制性。金属含量对发光菌活性影响相关性的相关系数的绝对值越大,发光菌受到的毒性越大[28]。因此,发光菌对淋出液中不同重金属元素的敏感性表现为Zn>Pb>Mn>Fe>Cu>Cd,其中Zn、Pb、Mn等3种重金属的相关性最高,对明亮发光杆菌的生物活性起主要的抑制作用。
表7 重金属含量对明亮发光杆菌活性影响相关性
Table 7 Correlation of heavy metal content on activity of luminescent bacillus
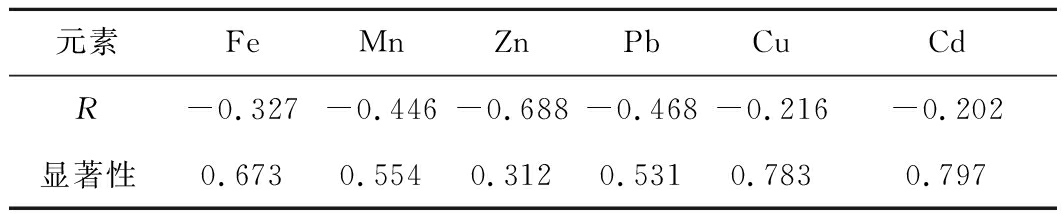
元素FeMnZnPbCuCdR-0.327-0.446-0.688-0.468-0.216-0.202显著性0.6730.5540.3120.5310.7830.797
1)不同固液比条件下煤矸石静态淋出液的pH、硫酸根以及重金属含量不同。固液比越大,静态淋出液的pH、硫酸根以及Fe、Mn元素的含量越大;淋溶过程中重金属元素Zn、Pb、Cu、Cd的溶出量随固液比的增加并未表现出明显的增加;不同粒径煤矸石浸出液的pH及各重金属元素的溶出量在短期内的波动性较大,大粒径煤矸石的金属溶出率最低,中粒径略大于小粒径。
2)动态淋溶时,随着淋溶时间的增加,不同粒径的煤矸石淋出液pH值随之不断增加,硫酸根、重金属元素随之呈现出较为明显的下降趋势。不同粒径的煤矸石其重金属元素的累计释放量也不同,中粒径的Fe、Mn累计释放量最大;小粒径的Zn、Cu、Cd累计释放量最大。重金属的溶出量与淋溶时间呈多项式关系,煤矸石中重金属的释放速率并未因粒径不同而表现出明显的变化。根据拟合方程可知煤矸石在堆放过程中的重金属释放会日渐平衡。
3)通过明亮发光杆菌T3对淋溶3 h时的淋溶液进行了生物毒性分析。样品溶液未稀释时呈剧毒状态,稀释100倍后不同粒径淋溶液的相对发光强度在56%~65%,中粒径淋溶液的发光强度为56%,毒性相对较大。相关性分析表明6种重金属均对发光菌的活性表现出抑制性,Zn、Pb、Mn等3种重金属起主要抑制作用。
[1] 雷建红.煤矸石的污染危害与综合利用分析[J].能源与节能,2017(4):90-91.
LEI Jianhong. Analysis of pollution hazards and comprehensive utilization of coal gangue[J]. Energy and Energy Conservation,2017(4):90-91.
[2] 张思思,陈旭峰,李春萍,等.尾矿及其浸出液中重金属形态分析与评价[J].应用化工,2017,46(6):1108-1112.
ZHANG Sisi, CHEN Xufeng, LI Chunping, et al. Speciation analysis and evaluation of heavy metals in tailings and its leaching solution[J]. Applied Chemical Industry, 2017,46(6):1108-1112.
[3] 郑永红,张治国,姚多喜,等. 煤矿复垦区土壤重金属含量时空分布及富集特征研究[J].煤炭学报, 2013,38(8): 1476-1483.
ZHENG Yonghong,ZHANG Zhiguo,YAO Duoxi, et al. Characteristics of temporal-spatial distribution and enrichment of heavy metals in coal mine reclaimed soil[J]. Journal of China Coal Society, 2013,38(8): 1476-1483.
[4] 张燕青,黄满红,戚芳方,等.煤矸石中金属和酸根离子的淋溶特性[J].环境化学,2014,33(3):452-458.
ZHANG Yanqing, HUANG Manhong, QI Fangfang, et al. The leaching characteristics of metals and acid radical ions in gangue[J]. Environmental Chemistry, 2014,33(3):452-458.
[5] 刘慧力,崔龙鹏.淮南矿区水体沉积物中金属污染及环境现状评价[J].环境科学研究,2009,22(5):601-606.
LIU Huili, CUI Longpeng. Assessment of pollution and environmental status of metals in sediments of Subsidence-Land-Water-Ponds in Huainan mining area[J]. Research of Environmental Sciences,2009,22(5):601-606.
[6] 王 萍,胡振琪,马保国,等.煤矸石浸水后pH值测定方法及结果比较[J].煤炭科学技术,2010,38(2):108-112.
WANG Ping, HU Zhenqi, MA Baoguo, et al. Comparison on pH value measuring methods and results of coal rejects after immersion in water[J]. Coal Science and Technology,2010,38(2):108-112.
[7] 赵洪宇,李玉环,宋 强,等.煤矸石动态循环淋溶液的特性[J].环境工程学报,2017,11(2):1171-1177.
ZHAO Hongyu, LI Yuhuan, SONG Qiang,et al. Characteristics of dynamic cyclic percolation solution from coal gangue[J]. Chinese Journal of Environmental Engineering, 2017,11(2):1171-1177.
[8] ALTAS Levent. Inhibitory effect of heavy metals on methane-producing anaerobic granular sludge[J]. Journal of Hazardous Materials,2009,162(2-3):1551-1556.
[9] CHANG W C, HSU G S, CHIANG S M, et al. Heavy metal removal from aqueous solution by wasted biomass from a combined AS-biofilm process.[J]. Bioresource Technology,2006,97(13): 1503-1508.
[10] FULLADOSA E, MURAT J C, MARTINEZ M, et al. Patterns of metals and arsenic poisoning in Vibrio fischeri bacteria.[J]. Chemosphere,2005,60(1):43-48.
[11] 张国辉. 镉的土壤微生物效应及发光细菌检测研究[D].呼和浩特:内蒙古大学,2009.
ZHANG Guohui. Effeet of heavy metal cadmium on soill microbiologieal activities and luminescent bacteria toxicity test[D].Huhehaote: Inner Mongolia University,2009.
[12] QU Ruijuan, WANG Xinghao, LIU Zhengtao, et al. Develop-ment of a model to predict the effect of water chemistry on the acute toxicity of cadmium to Photobacterium phosphoreum[J]. Journal of Hazardous Materials,2013,262:288-296.
[13] BIBISAIMA Zeb, ZHENG Ping, QAISAR Mahmood, et al. Assessment of combined toxicity of heavy metals from industrial wastewaters on Photobacterium phosphoreum T3S[J]. Applied Water Science,2017,7(4):2043-2050.
[14] 徐恒蒲,孟一鸣,李 澳,等.重金属污染土壤生物毒性的发光菌法测定及评价[J].化工环保,2019,39(5):538-544.
XU Hengpu, MENG Yiming, LI Ao, et al. Detection and evaluation of biotoxicity of heavy metal-contaminated soil using Photobacterium phosphoreum[J]. Environmental Protection of Chinese of Chemical Industry, 2019,39(5):538-544.
[15] 隋成瑶.发光细菌法在环境监测中的应用[J].黑龙江环境通报,2018,42(3):23-25.
SUI Chengyao. Application of luminescent bacteria method in environment monitoring[J]. Heilongjiang Environmental Journal, 2018,42(3):23-25.
[16] 许春燕,安晓雯,王乐雪,等.发光细菌在环境生物毒性检测中的应用[J].辽宁化工,2018,47(3):256-258.
XU Chunyan, AN Xiaowen, WANG Lexue, et al. Application of luminescent bacteria in the detection of environmental biological toxicity[J]. Liaoning Chemical Industry, 2018,47(3):256-258.
[17] 国家环境保护局科技标准. 水质急性毒性的测定发光细菌法:GB/T 15441—1995[S]. 北京:中国环境科学出版社, 1995.
National Environmental Protection Agency Technology Standard. Water quality-determination of the acute toxicity-Luminescent bacteria test. GB/T 15441—1995[S]. China: Environmental Science Press,1995.
[18] ZHANG Hongjian,OUYANG Sailan. Release characteristics of heavy metals from coal gangue under simulation leaching conditions[J]. Energy Exploration & Exploitation,2014,32(2):413-422.
[19] 肖利萍,梁 冰,陆海军,等.煤矸石中某些物淋溶释放特点的实验分析[J].安全与环境学报,2006(2):19-22.
XIAO Liping,LIANG Bing,LU Haijun,et al.Analysis of characteristics of leaching release of some substances in coal gangue[J]. Journal of Safety and Environment, 2006(2):19-22.
[20] ASHFAQ M, HEERALAL M, MOGHAL A A B. Effect of coal gangue particle size on its leaching characteristics[C]//Geo-Congress 2020: Geo-Systems, Sustainability, Geoenvironmental Engineering, and Unsaturated Soil Mechanics, Reston, VA: American Society of Civil Engineers, 2020: 107-114.
[21] 林 海,李 洁,董颖博.粒度对石煤钒矿废石重金属静态淋溶的影响规律[J].稀有金属,2017,41(6):693-700.
LIN Hai, LI Jie, DONG Yingbo. Heavy metal static leaching rules affected by different particle sizes of vanadium waste rock[J]. Chinese Journal of Rare Metals, 2017,41(6):693-700.
[22] 何 保,李振南,董艳荣,等.煤矸石主要污染组分静态溶出规律研究[J].硅酸盐通报,2018,37(4):1441-1446.
HE Bao, LI Zhennan, DONG Yanrong, et al.Static leaching law of main pollution components of coal gangue[J]. Bulletin of the Chinese Ceramic Society, 2018,37(4):1441-1446.
[23] ASHFAQ M, LAL M H, MOGHAL A A B. Static and dynamic leaching studies on coal gangue[M]. Sustainable Environmental Geotechnics. Springer, Cham, 2020: 261-270.
[24] MOGHAL A A B. State-of-the-art review on the role of fly ashes in geotechnical and geoenvironmental applications[J]. Journal of Materials in Civil Engineering, 2017, 29(8): 04017072.
[25] 王心义,杨 建,郭慧霞.矿区煤矸石堆放引起土壤重金属污染研究[J].煤炭学报,2006,31(6):808-812.
WANG Xinyi, YANG Jian, GUO Huixia. Study on heavy metals in soil contaminated by coal waste rock pile[J].Journal of China coal society, 2006,31(6):808-812.
[26] 李万鹏. 淋滤作用下煤矸石中污染物质的释放机理及潜在生态风险评价[D].西安:长安大学,2017.
LI Wanpeng. Release mechainsm and potential ecological risk assessment of pollutants in coal gangue under leaching[D].Xi’an:Chang’an University,2017.
[27] 张敬凯,王春红,姚文博,等.煤矸石在动态淋溶条件下重金属的溶出特性[J].煤炭技术,2018,37(12):323-325.
ZHANG Jingkai, WANG Chunhong, YAO Wenbo, et al. Charactertics of heavy metal element dissolution of coal gangue under dynamic leaching condition[J]. Coal Technology, 2018,37(12):323-325.
[28] 杨丰隆,云 洋,武冬梅,等.矸石山及其下游土壤浸出液生物毒性研究[J].山西大学学报(自然科学版),2016,39(2):325-332.
YANG Fenglong,YUN Yang,WU Dongmei, et al. Biological toxicity studies of coal gangue and its downstream soil leachates[J]. Journal of Shanxi University (Natural Science Edition) ,2016,39(2):325-332.
