0 引 言
煤沥青(CTP)是煤焦油蒸馏产量最大的产品,我国每年产量约800万t。CTP虽被广泛应用于生产各种碳材料粘结剂、煤沥青涂料、铝电解电极、筑路和建筑等,但其大规模应用的缺乏导致我国CTP产能过剩。CTP含较多具有致癌性质的多环芳烃[1-2],随着人们环保意识的增强,CTP对环境和人类健康的潜在危害成为限制其应用的主要原因[3]。例如,近年来报道美国中东部一些城市由于应用掺有CTP的产品做密封涂层使城市周围水中沉淀物、土壤、停车场和街道尘埃中含有大量的毒性多环芳烃。因此,美国多州采取相应措施限制CTP应用[4-6]。当前如何降低或抑制CTP中毒性多环芳烃(PAHs)的释放已成为亟待解决的问题,但相关文献对之报道较少[7-8]。ZIELINSK等[9]用不饱和聚酯树脂、聚乙二醇等在140~160 ℃条件下与CTP反应,推测发生氧烷基化反应使CTP中苯并[a]芘(BaP)质量分数减少90%以上,但140~160 ℃的反应温度会使CTP释放出有毒挥发物。采用高锰酸钾氧化和溶剂萃取[10]处理CTP,可有效降低其中毒性多环芳烃质量分数82%以上,但氧化处理后的CTP应用性能变差。FENG等[11]采用10-十一烯醛为改性剂、硫酸氢钾为催化剂,在常压低温条件下改性CTP,使美国环保局(EPA)优先监控的16种致癌性多环芳烃脱除率达91%,但其所需反应时间在实际应用中过长而使效率变低。因此,在FENG等[11]工作的基础上,采用微波和紫外辅助改性缩短反应时间,提高CTP中EPA优先监控的16种多环芳烃脱除率,解释CTP和改性剂可能发生的反应机理,为后续CTP改性试验奠定理论研究基础。
1 煤沥青改性试验
1.1 煤沥青的微波/紫外改性试验
试验所用煤沥青为中温煤沥青,将其粉碎过筛至粒径<0.074 mm,室温下风干2 d,装入棕色瓶密封备用。
称取10 g筛选好的煤沥青、质量分数为8%的10-十一烯醛和质量分数为5%的KHSO4催化剂(基于CTP)与100 mL环己烷在广口瓶中混合均匀,加入磁子并将广口瓶置于装有水的烧杯中浸泡。随后将整个烧杯放入型号为XH-300UL的微波/紫外反应器中,在微波和/或紫外辐射下反应20~150 min,筛选最佳反应条件。微波加热反应过程中,微波功率保持在200 W,当反应温度达50 ℃时,自动调节至88~120 W,搅拌速度为900 r/min。紫外功率为250 W,波长为365 nm。反应结束后,旋蒸回收溶剂。将残留物在50 ℃条件下真空干燥至恒定质量,环己烷索式抽提并采用气相色谱(GC)分析[11]。3次平行试验后测量PAHs的质量浓度平均值。根据文献[12],以BaP的当量毒性(BaPeq)来比较改性前后CTP毒性,计算公式为
BaPeq=∑(ρ(PAHi)×RPFi)
其中:ρ(PAHi)为CTP中各种PAHs的质量浓度,mg/g;RPFi为不同PAHs所对应的毒性当量因子。使用多种评价毒性当量因子的方法(EPA、Wiles、OEHHA、KSIR、USFDA)来计算改性前后CTP的毒性。
1.2 煤沥青和改性煤沥青的基本性质
CTP改性前后的基础性质见表1。试验所有试剂均为分析纯。EPA优先监控的16种毒性多环芳烃标准样品分别为:萘(NAP)、苊(ACY)、苊烯(ACP)、芴(FLR)、菲(PHE)、蒽(ANT)、荧蒽(FLT)、芘(PYR)、苯并[a]蒽(BaA)、□(CHR)、苯并[k]荧蒽(BkF)、苯并[b]荧蒽(BbF)、苯并[a]芘(BaP)、茚并[1,2,3-cd]芘(IcP)、二苯并[a,h]蒽(DhA)、苯并[g,h,i]苝(BgP)。
表1 煤沥青(CTP)和改性后煤沥青(MCTP)的基础性质
Table1 Characteristics of CTP and modified CTP (MCTP)
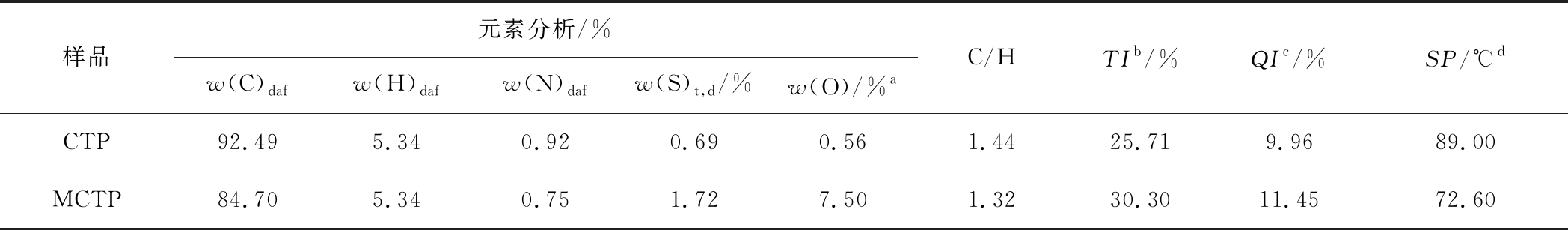
样品元素分析/%w(C)dafw(H)dafw(N)dafw(S)t,d/%w(O)/%aC/HTIb/%QIc/%SP/℃dCTP92.495.340.920.690.561.4425.719.9689.00MCTP84.705.340.751.727.501.3230.3011.4572.60
注:a基准不同;b甲苯不溶物; c喹啉不溶物;d环球法
1.3 煤沥青和改性煤沥青的性质表征
采用与文献[11]相类似的抽提测试方法表征改性前后CTP特征。试验过程如下:用环己烷索式抽提CTP至无色,并对回流液进行浓缩定容。采用0.22 μm 有机滤头过滤CTP定容液,采用气相色谱仪(Agilent 7820A)检测PAHs。试验时,色谱柱为19091J-413 HP-5(30.0 m×0.25 mm ID×0.25 μmdf),载气为30 mL/min高纯 N2。首先以100 ℃恒温3 min,再以5 ℃/min速率升至300 ℃,300 ℃恒温10 min,进样口温度为300 ℃,分流比10∶1。采用外标法对16种PAHs进行定量分析,测量3次计算平均值。红外(FTIR)分析采用IRAFFINITY-1型傅里叶变换红外光谱仪。测试条件如下:分辨率4.0 cm-1,扫描频率为36次/s,扫描范围400~4 000 cm-1。拉曼(Raman)分析采用HORIAB HR800共聚焦显微拉曼光谱仪。试验条件如下:激发波长532 nm,积分时间20 s,光斑尺寸2 μm,光谱范围100~4 000 cm-1。高分辨固体13C核磁共振(13C CP/MAS NMR)分析采用Bruker AVWB III 600 M型波谱仪。分析测试条件如下:共振频率为150.9 MHz,转速为10 kHz,极化时间为2 ms,延迟时间为3 s,采集8 000次。X射线衍射(XRD)分析采用Rigaku D/max 2500型X射线衍射分析仪。分析测试条件如下:Cu靶Kα射线(λ= 1.540 56Å),Ni滤波片,管电压为40 kV,管电流为30 mA;连续扫描,步长为0.01,速率为8(°)/min,扫描范围2θ=5°~85°。
2 结果与讨论
2.1 试验结果分析
图1为不同条件下16种PAHs的脱除率。由图1可知,单独微波或单独紫外条件下,EPA优先监控的16种毒性PAHs在60~90 min内脱除率都可达到最高(微波90.96%和紫外90.37%)。相比常温加热改性CTP反应[11],微波或紫外辅助可将反应时间缩短2.5~3.0 h。微波和紫外同时辅助改性CTP脱除PAHs时,最大脱除率出现在120 min,反应时间超出单独微波(60 min)或单独紫外(90 min)辅助改性,这可能是由反应过程中微波和紫外相互作用导致。随着改性时间增加,PAHs脱除率明显降低,可能是因为碳正离子稳定性变差导致改性剂活性降低。MCTP中16种EPA优先监控的毒性PAHs脱除率最高为91.59%,略高于无微波和紫外辅助改性试验(91.10%)[11],16种毒性PAHs的总质量浓度降低为7.5 mg/g,且每种毒性PAHs质量浓度变化趋势与未经辅助改性试验结果趋势一致(图2)。不同毒性PAHs对人体健康影响有所差异,其相对毒性可根据苯并[a]芘毒性当量(BaPeq)来计算[12]。
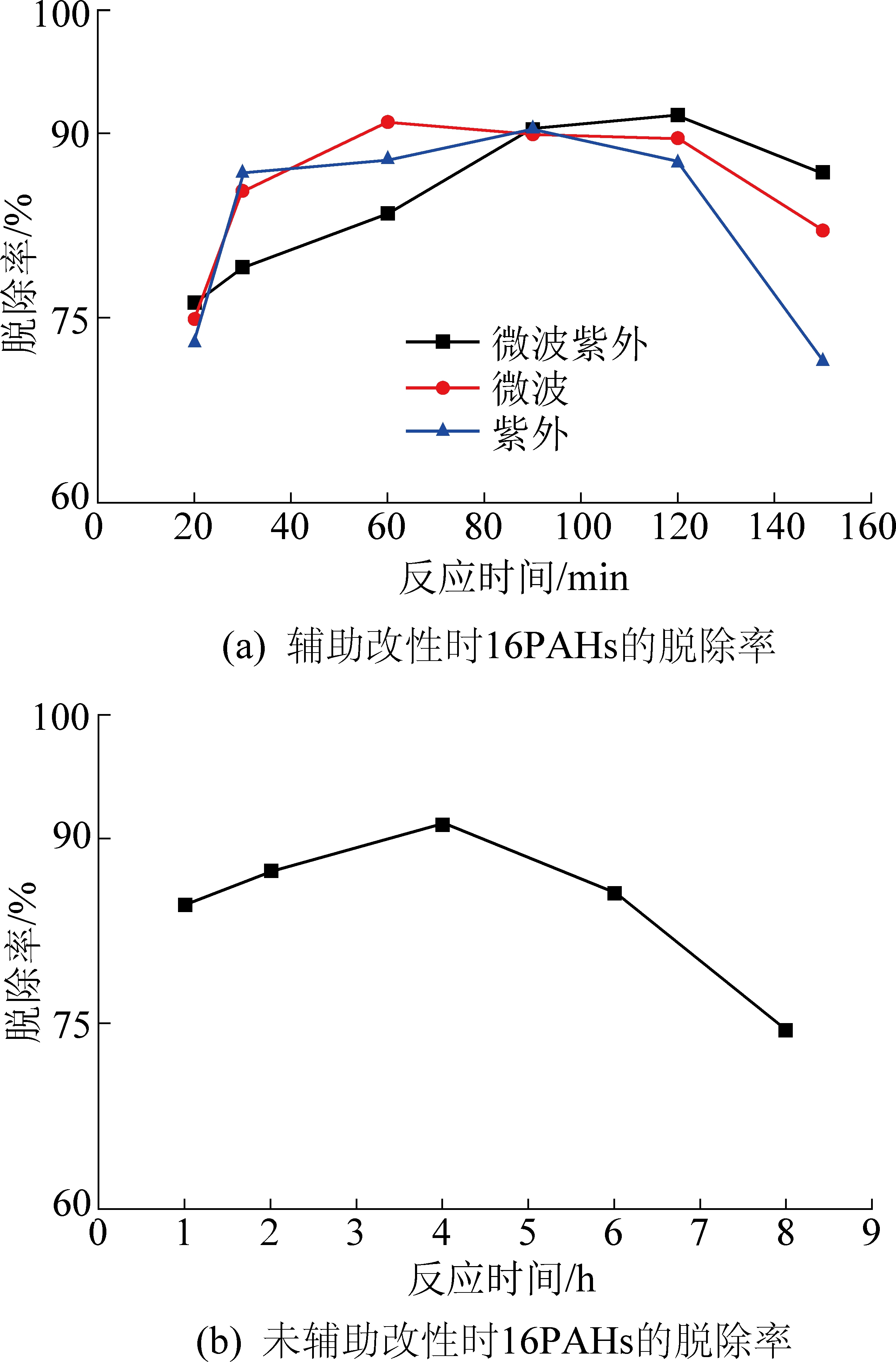
图1 不同条件下16种PAHs的脱除率
Fig.1 16 PAHs reduction efficiency variation with different conditions
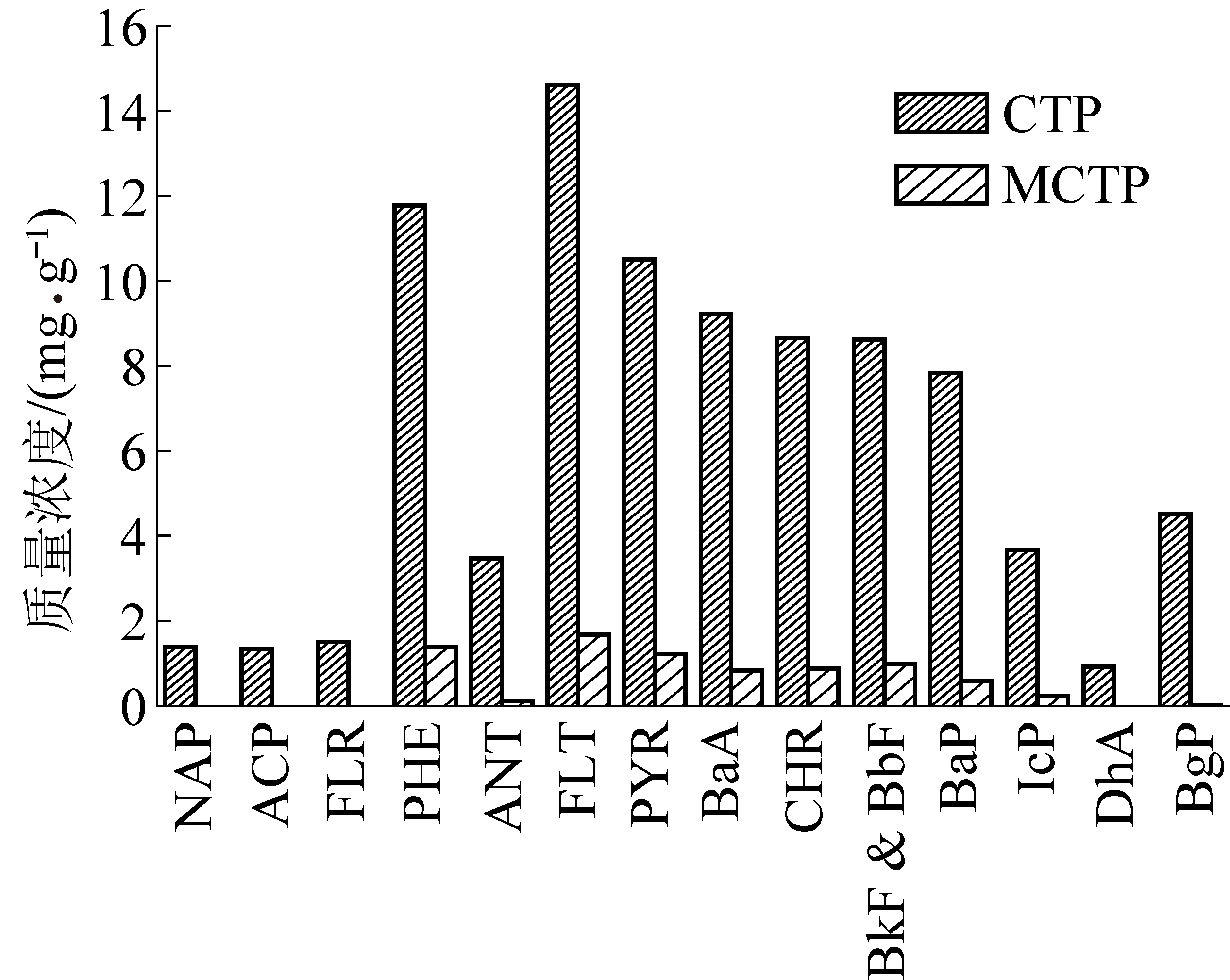
图2 改性前后16种PAHs在CTP中的质量浓度
Fig.2 16 priority PAHs concentration comparison in CTP and MCTP
图3为煤沥青改良前后(CTP和MCTP)的苯并[a]芘毒性当量(BaPeq)比较,由图3可知,不同计算方法算得毒性PAHs的BaPeq差异较大,但总体来说,MCTP中PAHs的BaPeq都远小于CTP中PAHs的BaPeq。其中采用Wiles方法计算时,BaPeq从17.50 mg/g降至0.97 mg/g,BaPeq降低率最大,说明微波和紫外辅助改性CTP效果显著。后续表征分析时,MCTP为微波和紫外同时辅助改性120 min后的CTP。

图3 煤沥青改良前后(CTP和MCTP)的苯并[a]芘毒性当量(BaPeq)比较
Fig.3 Comparison of contents of toxic PAHs BaPeq values in CTP and MCTP
2.2 改性前后煤沥青性质的表征分析
2.2.1 红外光谱分析
图4为CTP、MCTP和改性剂10-十一烯醛的红外分析谱图。由图4可知,2 700~2 980 cm-1和1 480~1 370 cm-1峰值处均为脂肪族结构的特征峰[13-14],MCTP特征峰有所增强,说明MCTP脂肪族结构含量高于CTP。1 690~1 720 cm-1处为10-十一烯醛典型C![]() O结构特征峰,MCTP在1 690~1 720 cm-1处C
O结构特征峰,MCTP在1 690~1 720 cm-1处C![]() O特征峰峰强减弱变不明显,推测10-十一烯醛与CTP发生反应。750 cm-1为取代芳环上C—H的面外弯曲振动吸收峰[15],图4知10-十一烯醛参与反应使C—H吸收峰增强,推测多环芳烃在反应过程可能发生了部分取代反应。
O特征峰峰强减弱变不明显,推测10-十一烯醛与CTP发生反应。750 cm-1为取代芳环上C—H的面外弯曲振动吸收峰[15],图4知10-十一烯醛参与反应使C—H吸收峰增强,推测多环芳烃在反应过程可能发生了部分取代反应。
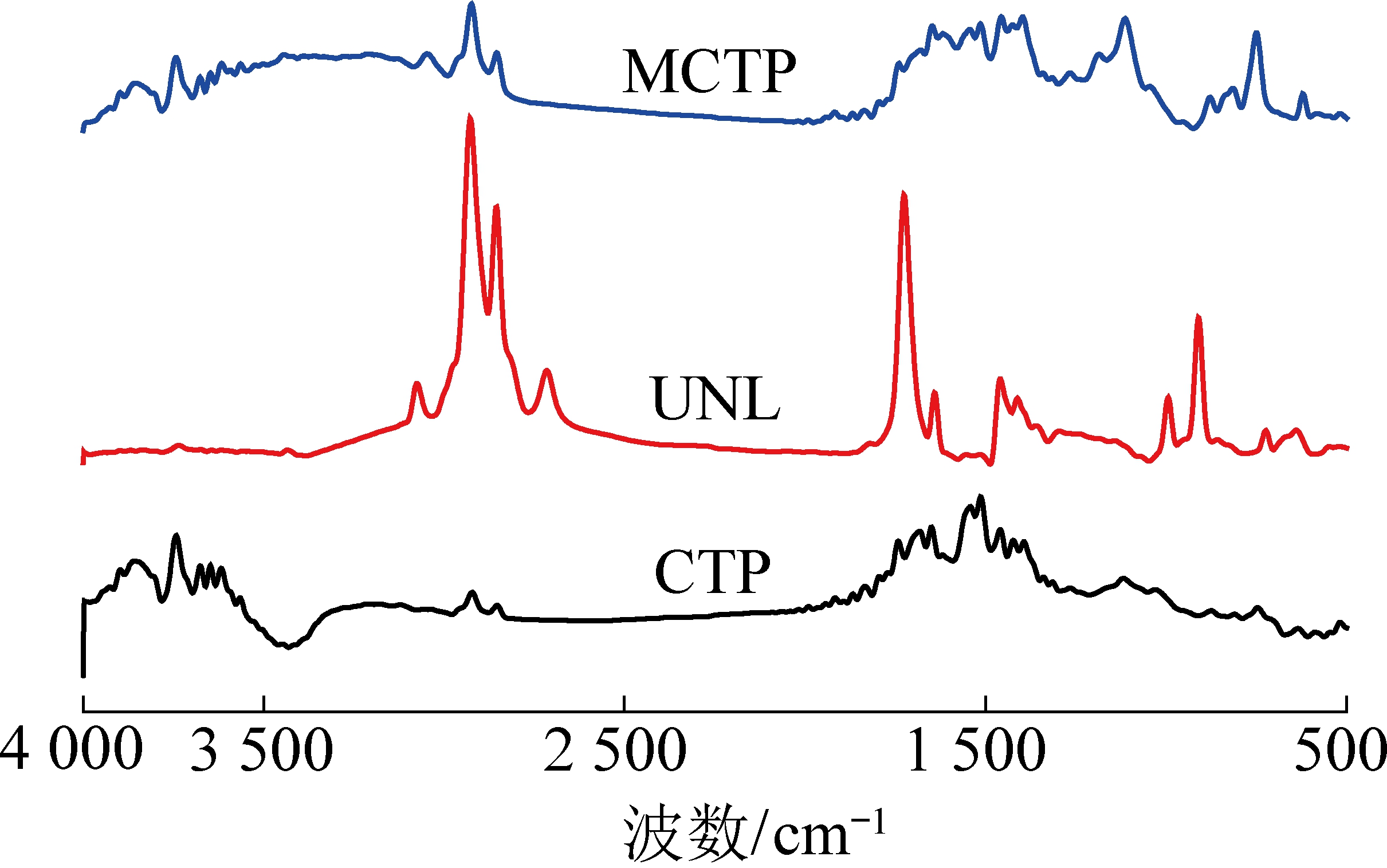
图4 煤沥青(CTP)、改性后煤沥青(MCTP)和改性剂10-十一烯醛的红外分析谱
Fig.4 FT-IR spectra of CTP,MCTP and modifier of 10-undecenal (UNL)
2.2.2 拉曼光谱分析
拉曼光谱是很好的表面表征技术,可以提供详细的碳材料微光结构信息[16]。煤沥青的特征拉曼光谱存在两个区域,分别为一级模(800~2 000 cm-1)和二级模(2 400~3 400 cm-1)区域[17]。对其一级模区域进行研究,采用Peakfit软件对CTP和MCTP的特征拉曼谱图进行分峰拟合,5个峰分别为:D1峰(~1 350 cm-1)、D2峰(~1 465 cm-1)、D3峰(~1 240 cm-1)、D4峰(~1 100 cm-1)和G峰(~1 590 cm-1)[18-20]。为提高谱图参数的准确性,应用洛伦兹-高斯曲线对其进行拟合,如图5所示。CTP的一阶拉曼谱带和振动模式以及CTP和MCTP的拉曼光谱参数分别见表2和表3[21-22]。
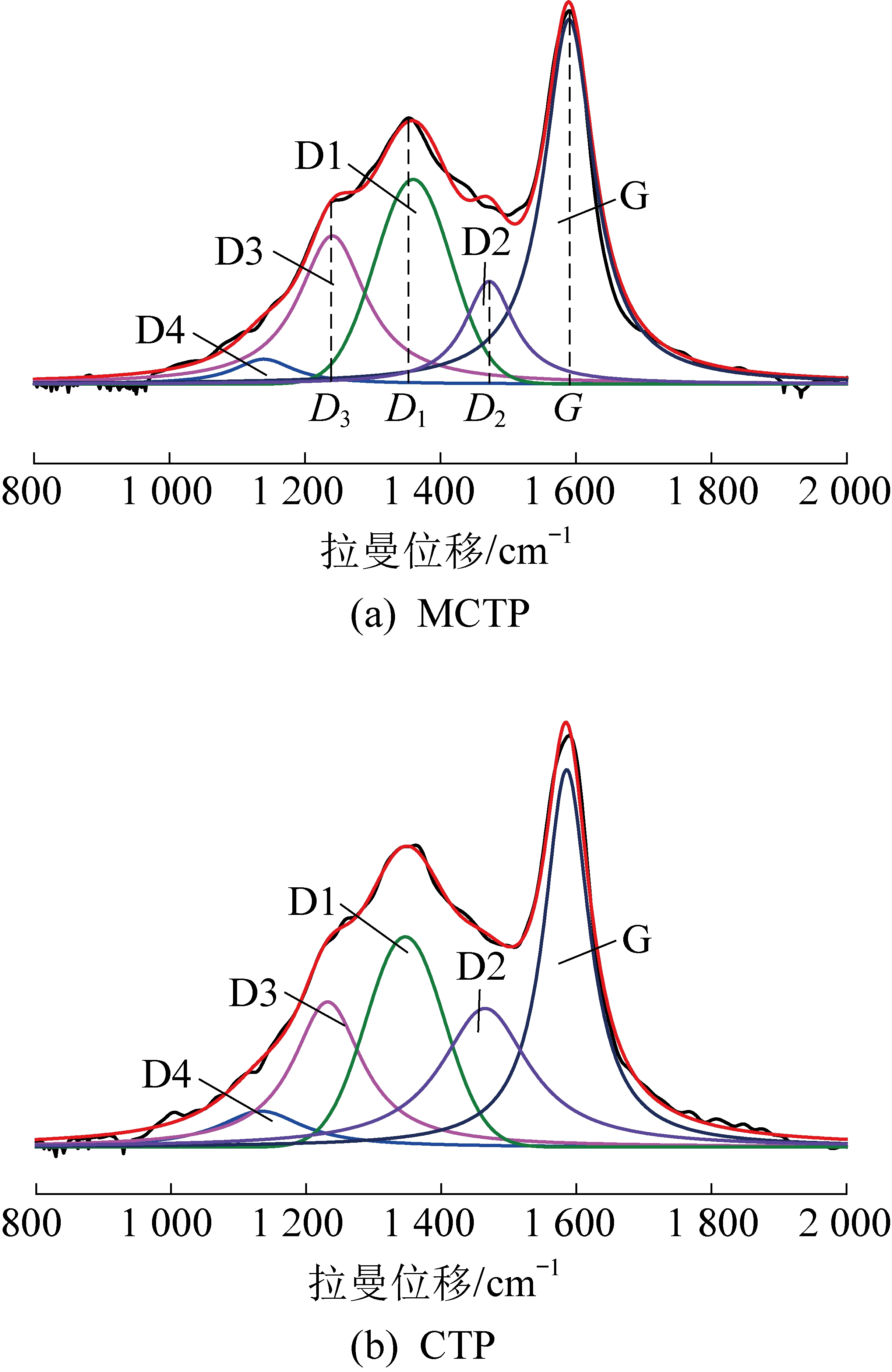
图5 煤沥青(CTP)和改性后煤沥青(MCTP)的一阶拉曼光谱带曲线拟合
Fig.5 Curves fit with band combination for the first-order Raman spectra of CTP and MCTP
表2 CTP中一阶拉曼光谱带及其振动模式
Table 2 First-order Raman bands and vibration modes reported for coal tar pitch

谱带名称拉曼位移/cm-1描述键型D1~1 350芳环及不少于6个环的芳香族化合物之间的C—C键振动 SP2D2~1 465亚甲基或甲基;脂肪烃的振动;非晶碳结构SP2,SP3D3~1 240芳基-烷基醚;准芳香族化合物;脂肪结构或类烯烃结构中C—C键振动SP2,SP3D4~1 100芳环上的C—H键振动;临位二取代苯环SP2G~1 590石墨特征峰,E2g 对称性;芳环呼吸振动,CC键振动SP2
由图5可知改性后,CTP的D1峰和G峰有分别向高频范围和低频范围移动的趋势,并且MCTP的峰位差(G-D1)变小。可以推测改性后CTP中碳含量减少,这与CTP基础性质分析得到结果一致(表1)。MCTP半峰宽比(G/D1)明显增加,可推测大分子结构中烷基(—CH3,—CH2)形成的烃类侧链(即脂肪族)与部分含氧官能团(C![]() O,C—O和—OH等)有更多生成,脂肪族占比增加。反应在宏观现象上为MCTP的软化点降低,这与表1中结果相符合。通过比较改性前后CTP的D1峰和G峰的峰面积比(AD1/AG)发现,MCTP的有序结构减少、石墨化程度变小,同时脂肪族占比增加,可推测10-十一烯醛改性CTP过程中与PAHs发生亲电取代反应。
O,C—O和—OH等)有更多生成,脂肪族占比增加。反应在宏观现象上为MCTP的软化点降低,这与表1中结果相符合。通过比较改性前后CTP的D1峰和G峰的峰面积比(AD1/AG)发现,MCTP的有序结构减少、石墨化程度变小,同时脂肪族占比增加,可推测10-十一烯醛改性CTP过程中与PAHs发生亲电取代反应。
表3 CTP和MCTP拉曼参数
Table 3 Raman spectral parameters of the studied CTP and MCTP
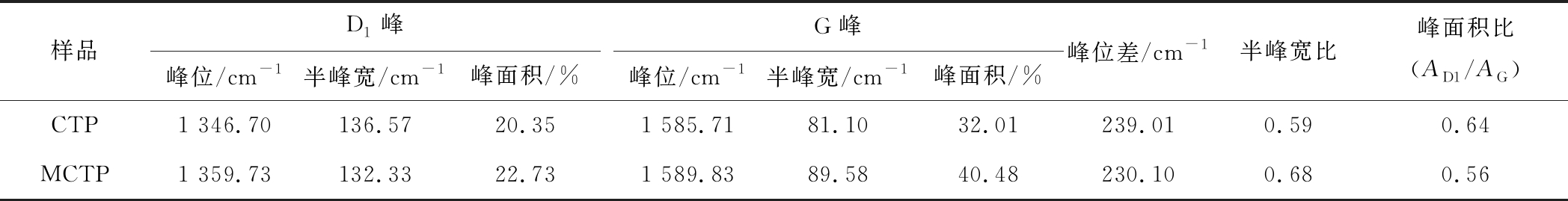
样品D1峰峰位/cm-1半峰宽/cm-1峰面积/%G峰峰位/cm-1半峰宽/cm-1峰面积/%峰位差/cm-1半峰宽比峰面积比(AD1/AG)CTP1 346.70136.5720.351 585.7181.1032.01239.010.590.64MCTP1 359.73132.3322.731 589.8389.5840.48230.100.680.56
2.2.3 高分辨固体13C核磁共振分析
改性前后CTP的固体13C CP/MAS NMR 图谱如图6所示。在δ为22~34.3化学位移的峰群,亚甲基碳、次甲基碳结构为此区间最强的共振信号。MCTP的峰群面积远大于CTP,MCTP的共振信号明显增强,说明MCTP比CTP含有更多的脂肪族链状亚甲基碳。对CTP和MCTP的固体13C CP/MAS NMR图谱中δ为100~165芳香碳结构区域的各峰进行标定和拟合,拟合曲线如图7所示。将各碳结构进行归属,最终利用拟合结果获得各碳的结构参数,见表4。
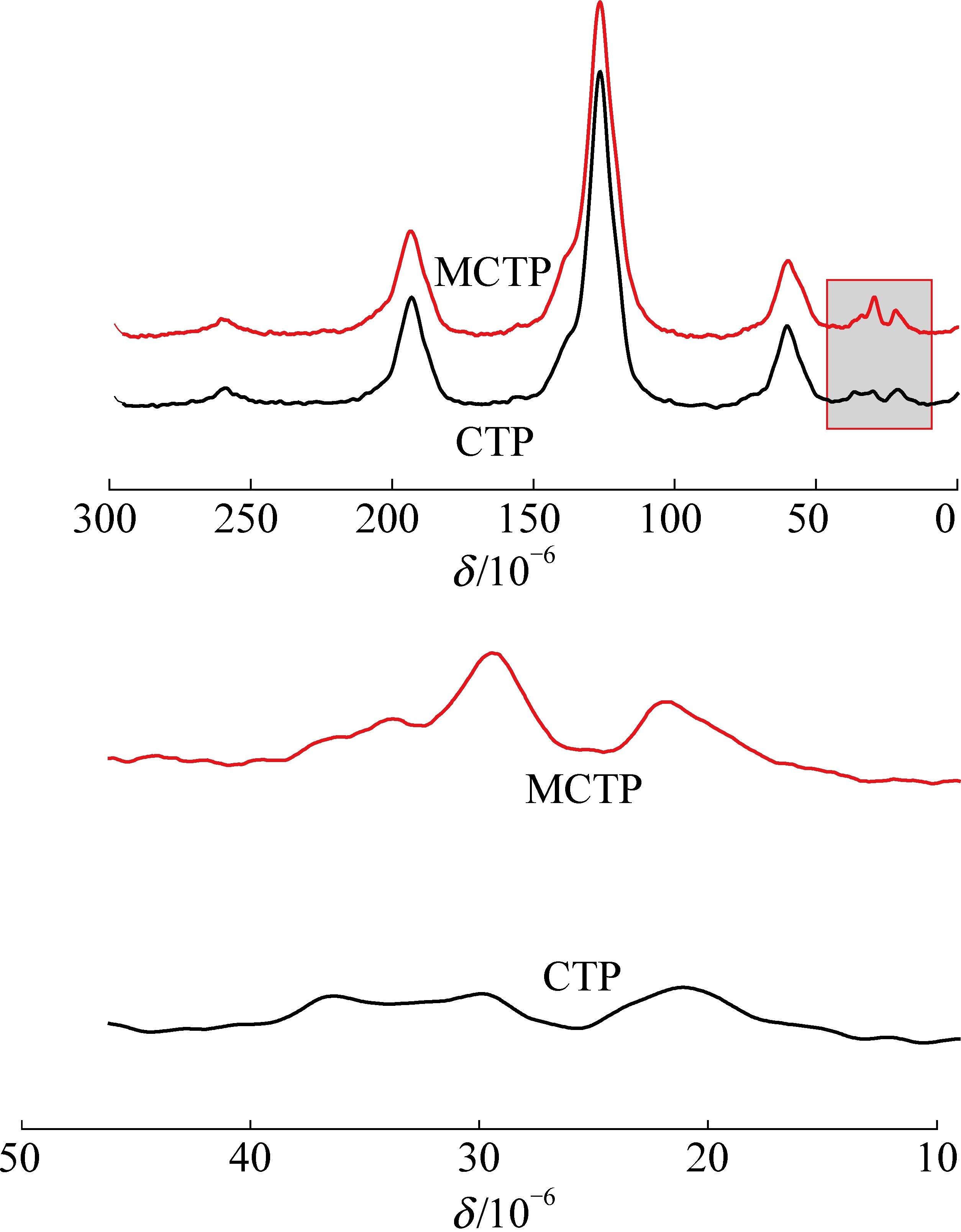
图6 CTP和MCTP的固体13C CP/MAS NMR图谱
Fig.6 Solid-state 13C CP/MAS NMR spectra of CTP and MCTP
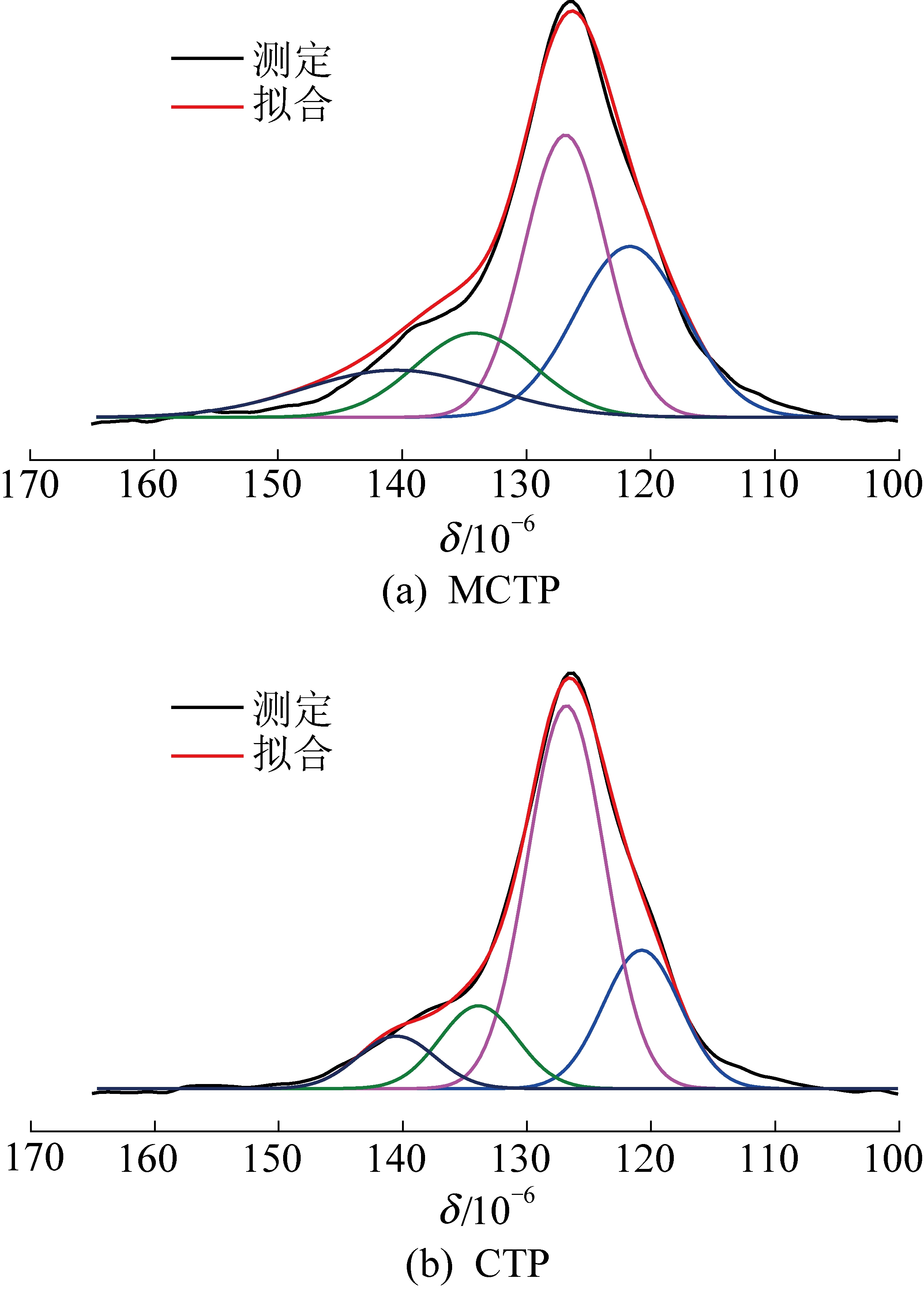
图7 CTP和MCTP的固体13C CP/MAS NMR拟合曲线
(1、2为芳香质子化碳;3为桥头芳碳;4为侧枝芳碳)
Fig.7 Fitting curves of Solid-state13C CP/MAS NMR spectra of CTP and MCTP(1、2:Aromatic protonated carbon;3:Bridging ring junction carbon;4:Aromatic branched carbon)
表4 CTP和MCTP的固体13C CP/MAS NMR中不同结构碳的化学位移值及含量
Table4 Chemical shift values and mole percent of different structural carbons in solid-state 13C NMR spectra of CTP and MCTP
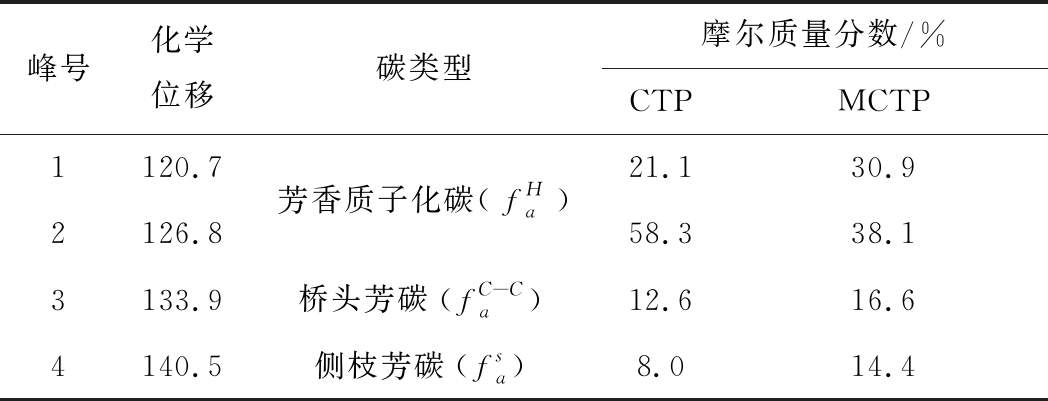
峰号化学位移碳类型摩尔质量分数/%CTPMCTP1120.72126.8芳香质子化碳(fHa)21.130.958.338.13133.9桥头芳碳(fC-Ca)12.616.64140.5侧枝芳碳(fsa)8.014.4
在CTP和MCTP中,芳香质子化碳的化学位移分别为120.7和126.8,占碳结构官能团绝大部分。
在MCTP中,位移为126.8的质子化芳碳率减少,位移为133.9桥头芳碳率和位移为140.5的侧枝芳碳率增约分别为4 mol%和6.4 mol%[23],这表明多环芳烃与改性剂之间发生了烷基化反应。芳香环取代度是CTP结构组成的重要结构参数[24],其计算公式为
式中:![]() 为芳香质子化碳,
为芳香质子化碳,![]() 为桥头芳碳,
为桥头芳碳,![]() 为侧枝芳碳,%。
为侧枝芳碳,%。
由计算得出CTP(δ)由8.0%增加到MCTP(δ)的14.4%。强化改性后,CTP的芳香取代度约增加6.4%,表明10-十一烯醛和毒性PAHs在侧枝芳香碳发生烷基化反应。
2.2.4 X射线衍射(XRD)
为确定强化改性前后CTP组分的晶型和组成,对其进行XRD分析并拟合曲线如图8所示,拟合结果见表5。MCTP的γ峰面积增加,002峰面积减小,芳香度由75.01%下降到71.25%,表明MCTP中脂肪族结构增加,使MCTP中毒性PAHs质量浓度减少,这与上述其他分析结果一致。
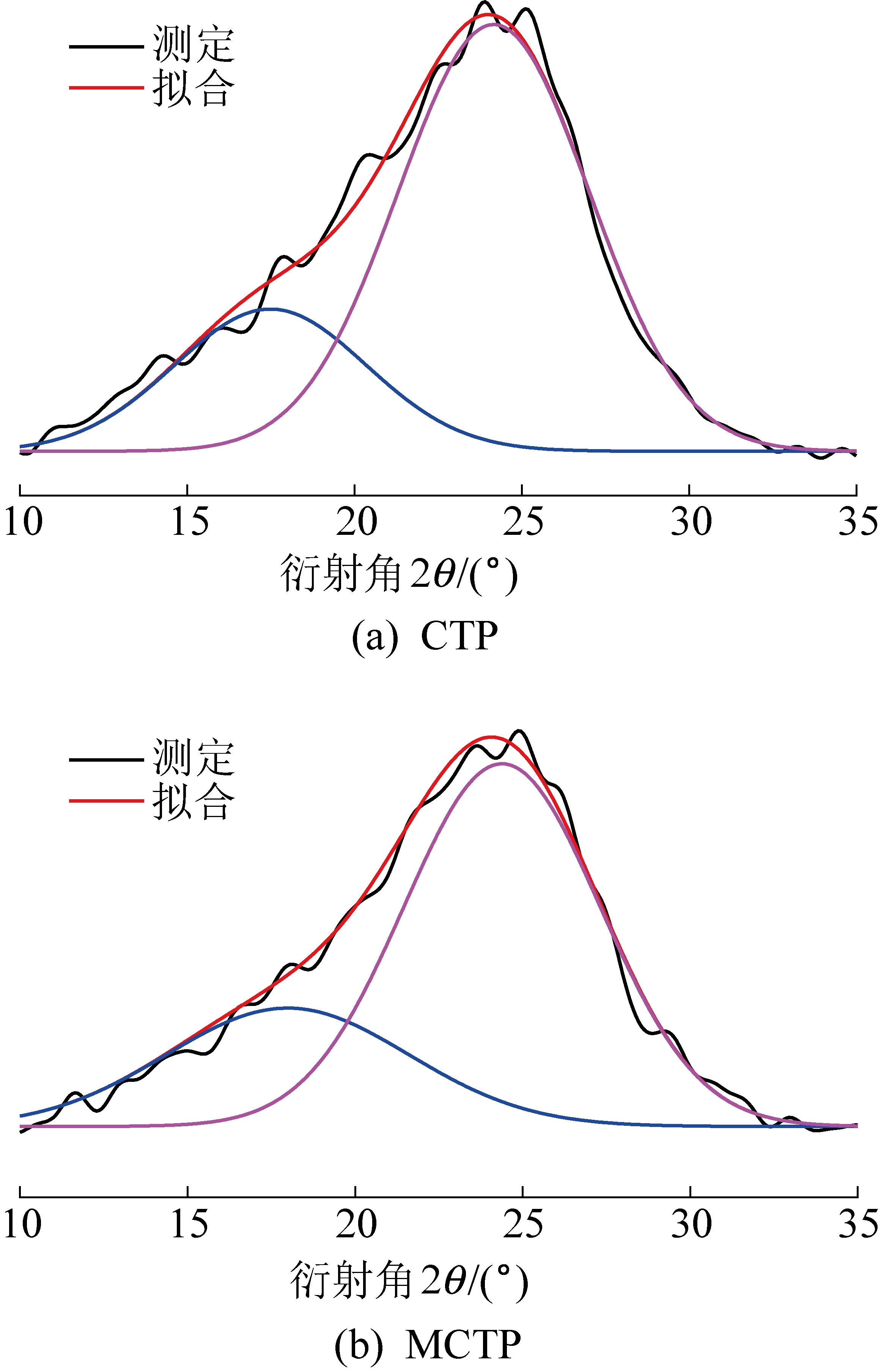
图8 CTP和MCTP的XRD拟合曲线
Fig.8 Fitting curves of XRD spectra of CTP and MCTP
表5 CTP和MCTP的XRD拟合曲线
Table5 Fitting curves of XRD spectra of CTP and MCTP

样品峰1峰2芳香度/%CTPMCTP002002γγ75.0171.25
3 结 论
1)采用微波和/或紫外来辅助改性CTP,以硫酸氢钾为催化剂、10-十一烯醛为改性剂对CTP进行改性来降低其中EPA优先监控的16种毒性多环芳烃,发现微波和紫外同时辅助改性效果(91.59%)优于单独微波(90.96)或紫外(90.37%)。
2)在60~120 min内,采用微波和/或紫外来辅助改性CTP可以达到最优效果,16种毒性多环芳烃(PAHs)总质量分数最大脱除率为91.59%,总质量分数小于7.41 mg/g,与无微波和紫外辅助改性相比,时间缩短了2~3 h,大幅提高了改性效率,且改性效果强于未辅助。
3)通过傅里叶变换红外光谱(FTIR)、拉曼光谱(Raman)、固体核磁共振碳谱(13C CP/MAS NMR)和X射线衍射(XRD)等表征分析改良前后的煤沥青,初步推测PAHs与改性剂部分发生烷基化反应,可降低CTP中毒性PAHs的质量分数。
[1] SCHREINERC A.Review of mechanistic studies relevant to the potential carcinogenicity of asphalts [J].Regulatory Toxicology and Pharmacology,2011,59(2):270-284.
[2] LI Z,WU Y,ZHAO Y,et al.Analysis of coal tar pitch and smoke extract components and their cytotoxicity on human bronchial epithelial cells[J].Journal of Hazardous Materials,2011,186(2/3):1277-1282.
[3] KIM K H,JAHAN S A,KABIR E,et al.A review of airborne polycyclic aromatic hydrocarbons (PAHs) and their human health effects[J].Environment International,2013,60:71-80.
[4] METRE P C V,MAHLER B J,WILSON J T.PAHs underfoot:contaminated dust from coal-tar sealcoated pavement is widespread in the United States[J].Environmental Science & Technology,2009,43(1):20-25.
[5] YANG Y,METRE P C V,MAHLER B J,et al.Influence of coal-tar sealcoat and other carbonaceous materials on polycyclic aromatic hydrocarbon loading in an urban watershed[J].Environmental Science & Technology,2010,44(4):1217-1223.
[6] MAHLER B J,METRE P C V,CRANE J L,et al.Coal-tar-based pavement sealcoat and PAHs:implications for the environment,human health,and stormwater management [J].Environmental Science & Technology,2012,46:3039-3045.
[7] AFANASOV I M,KEPMAN A V,MOROZOV V A,et al.Determination of polyaromatic hydrocarbons in coal tar pitch[J].International Journal of Analytical Chemistry,2009,64(4):361-365.
[8] SIDOROV O F.Reducing the carcinogenic impact of pitch processing[J].Coke and Chemistry,2013,56(2):63-69.
[9] ZIELIHSKI J,OSOWIECKA B,LISZYIISKA B,et al.Benzo[a]pyrene in coal tar pitch:chemical conversion in situ by alkylation[J].Fuel,1996,75(13):1543-1548.
[10] WANG W C,LIU G,SHEN J,et al.Reducing polycyclic aromatic hydrocarbons content in coal tar pitch by potassium permanganate oxidation and solvent extraction [J].Journal of Environmental Chemical Engineerin,2015,3(3):1513-1521.
[11] FENG Y H,WANG Y G,LIU G,et al.Modification of coal-tar pitch with 10-Undecenal to reduce the content of environmental pollutants of polycyclic aromatic hydrocarbons[J].Journal of Cleaner Production,2018,172:2544-2552.
[12] ALVAREZ P,GRANDA M,SUTIL J,et al.Preparation of low toxicity pitches by thermal oxidative condensation of anthracene oil[J].Environmental Science & Technologyl,2009,43(21):8126-8132.
[13] PAPOLE G,FOCKE W W,MANYALA N.Characterization of medium-temperature Sasol-Lurgi gasifier coal-tar pitch [J].Fuel,2012,98:243-248.
[14] ALCANIZMONGE J,CAZORLAAMOROS D,LINARESSOLANO A.Characterization of coal-tar pitches by thermal analysis infrared spectroscopy and solvent fractionation [J].Fuel,2001,80(1):41-48.
[15] GUILLEN M D,IGLESIAS M J,DOMINGUEZ A,et al.Semi-quantitative FTIR analysis of a coal-tar pitch and its extracts and residues in several organic solvents [J].Energy & Fuels,1992,6(4):518-525.
[16] MONTESMORAN M A,CRESPO J L,YOUNG R J,et al.Mesophase from a coal tar pitch:a Raman spectroscopy study[J].Fuel Process Technol,2002(77/78):207-212.
[17] BEYSSAC O,GOFFA B,PETITET J P,et al.On the characterization of disordered and heterogeneous carbonaceous materials by Raman spectroscopy [J].Spectrochim Acta Part A,2003,59(10):2267-2276.
[18] SADEZKY A,MUCKENHUBER H,GROTHE H,et al.Raman microspectroscopy of soot and related carbonaceous materials:spectral analysis and structural information [J].Carbon,2005,43(8):1731-1742.
[19] JAWHARI T,ROID A,CASADO J.Raman spectroscopic characterization of some commercially available carbon black materials[J].Carbon,1995,33(11):1561-1565.
[20] QUIRICO E,ROUZAUD J N,BONAL L,et al.Maturation grade of coals as revealed by Raman spectroscopy:progress and problems[J].Spectrochim Acta Part A,2015,61(10):2368-2377.
[21] LI X,HAYASHI J I,LI C Z.FT-Raman spectroscopic study of the evolution of char structure during the pyrolysis of a Victorian brown coal [J].Fuel,2006,85(12/13):1700-1707.
[22] DUN W,GUIJIAN L,RUOYU S,et al.Influences of magmatic intrusion on the macromolecular and pore structures of coal:Evidences from Raman spectroscopy and atomic force microscopy[J].Fuel,2014,119:191-201.
[23] MAJUMDAR R D,GERKEN M,HAZENDONK P.Solid-State 1H and 13C nuclear magnetic resonance spectroscopy of athabasca oil sands asphaltenes:evidence for interlocking π-stacked nanoaggregates with intercalated alkyl side chains[J].Energy & Fuels,2015,29(5):2790-2800.
[24] TONG J,HAN X,WANG S,et al.Evaluation of structural characteristics of Huadian oil shale kerogen using direct techniques (solid-state 13C NMR,XPS,FT-IR,and XRD)[J].Energy & Fuels,2011,25(9):4006-4013.
